Миграция водителя ритма по предсердиям
Потливость внезапная сильная
Постпрандиальная артериальная гипотония
Радиочастотная катетерная абляция (РЧА)
Синдром ранней реполяризации желудочков (РРЖ)
Систолическое (верхнее) артериальное давление
Соматизированная депрессия/тревога
Тромбоэмболия легочной артерии
Чрезпищеводное ЭФИ сердца
Аномально расположенная хорда (АРХ)
Артериальная гипертония беременных
Атриовентрикулярные реципрокные тахикардии
Гипертрофическая кардиомиопатия
Двухстворчатый аортальный клапан
Диастолическое (нижнее, "почечное") артериальное давление
Диастолическая дисфункция левого желудочка
Дисгормональная (климактерическая) кардиомиопатия
"Диффузные изменения в миокарде левого желудочка"
Кардиалгия - это любая боль за грудиной или в левой половине грудной клетки (в области сердца) отличная по своим характеристикам от стенокардии и, соответственно, не являющаяся симптомом ишемической болезни сердца. Этот термин, возможно, вам не так часто приходиться слышать, однако распространенность кардиалгия выше стенокардии. По моим наблюдениям в поликлинике при обращении пациентов с жалобами на боли в области сердца соотношение кардиалгии и стенокардии примерно 20:1. Кардиалгия часто выступает антиподом стенокардии, так как приходится проводить важнейшую дифференциальную диагностику по категории "опасная" боль (стенокардия) - "неопасная" боль (кардиалгия). Кардиалгия, хотя и может быть достаточно интенсивной, в подавляющем большинстве случаев угрозы не представляет.

Основная доля (90%) кардиалгий приходится на кардионевроз (особенно на фоне синдрома дисплазии соединительной ткани) и гипертоническую болезнь. В таком случае ее характеристики следующие:
- боль может быть любой по ощущениям (чаще ноет, колит, давит);
- чаще локализуется не за грудиной, а в прекордиальной области;
- длиться долго - часами или даже днями, иногда кратковременно "прокалывает";
- может отдавать в левое плечо и руку, вызывая ощущение онемение левой руки, пальцев кисти;
- нередко усиливается при глубоком дыхании, сопровождаясь чувством неудовлетворенного вдоха ("вздохи облегчения");
- для ее купирования могут быть эффективны успокаивающие (например, валидол, корвалол), а нитроглицерин бесполезен;
- она не связана с физической нагрузкой, наоборот, чаще возникает и усиливается в покое;
- хронологически появляется на фоне или после переживаний;
- может весьма красочно (вычурно) субъективно воспринимается - горячий шар в груди, ком в области сердца, что-то горячее внутри и т.д.
Хочу подчеркнуть (!), что при климактерическом и алкогольном поражении сердца характерологические особенности боли в прекардиальной области могут быть весьма схожи с выше описанными!
Кардиалгия является одним из возможных симптомов очень многих заболеваний (несколько десятков) и в большинстве случаев не опасна. Невротические расстройства (на их долю приходится 90% кардиалгий), пролапс митрального клапана, алкогольное поражение сердца, патология пищевода или желудка, межреберная невралгия, остеохондроз, мужской или женский климакс, опоясывающий герпес грудной клетки - это далеко неполный перечень заболеваний, которые могут проявляться болями в области сердца. Резюме: если вас беспокоит боль в области сердца, то высока вероятность того, что она либо не имеет отношения к сердцу, либо обусловлена кардионеврозом.
Артериальная гипертония - синдром, проявляющийся устойчивым или периодическим повышением кровяного артериального давления (АД). Известно, что верхней границей нормального АД являются цифры 135\85 мм.рт.ст. Нижняя граница нормы не столь очевидна, так как для некоторых лиц АД равное 90/60 мм. рт. ст. является индивидуальной нормой, а повышение его до 120/80 мм.рт.ст. сопровождается появлением неприятных ощущений. Тем не менее, АД ниже 105/60 мм.рт.ст. в целом не характерно для здорового человека. Величина АД зависит от трех физиологических параметров: частоты сердечных сокращений, тонуса периферических артерий, объема циркулирующей крови. Их вариация и будет определять текущее АД. Регуляторные механизмы человеческого организма слаженно контролируют уровень АД: например, уменьшение объема циркулирующей крови (обезвоживание, кровопотеря - ↓АД) сопровождается повышением тонуса периферических артерий (↑АД); патологически редкий ритм сердца (аритмия - ↓АД) приводит к рефлекторному повышению тонуса периферических артерий и задержки жидкости в организме (↑АД). При артериальной гипертонии происходит срыв регуляторных механизмов, когда наблюдается избыточное и стойкое превалирование одного или нескольких факторов, повышающих АД: например, длительный спазм периферических артерий. Чем опасен этот синдром? Артериальная гипертония 1) значительно ускоряет развитие атеросклероза (по-простому: старение сосудов), 2) повышает нагрузку на сердце, что со временем приводит к гипертрофии стенок левого желудочка и развитию сердечной недостаточности. Самые опасные осложнения артериальной гипертонии: инсульт или инфаркт - представляют непосредственную угрозу жизни.
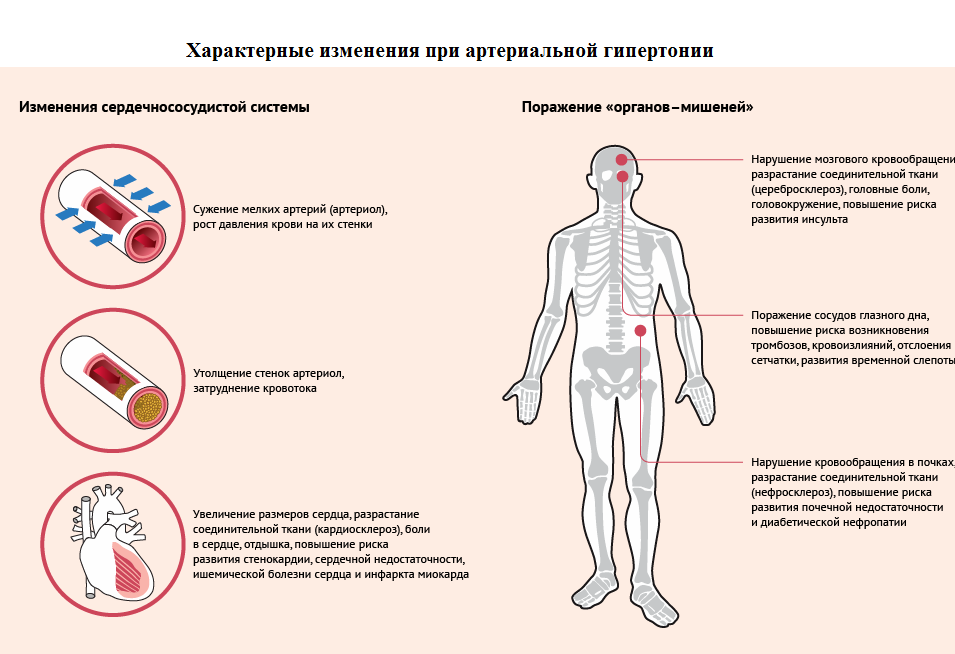
Коварство заболевания заключается в том, что человек может практически не ощущать повышенное АД. Факторы, являющиеся составной частью неправильного образа жизни - хронический стресс, неразрешившийся невроз, сидячий образ жизни, избыточный вес, длительное отсутствие отдыха (трудоголизм), контролирующий тип поведения - способствуют возникновению и закреплению артериальной гипертонии. Лечение артериальной гипертонии лекарствами может быть затруднительным, если причины, вызвавшие ее, не устранены. Артериальная гипертония - это синдром, который может быть составной частью одного из 3-х заболеваний: 1) гипертоническая болезнь (90%) - болезнь неправильного образа жизни; чаще всего в ее основе лежит хроническое эмоциональное перенапряжение с гневом подсознательно направленного вовнутрь (внутриличностный конфликт); 2) НЦД по гипертоническому типу (5%) - кардионевроз с гипертензивными реакциями; 3) вторичная артериальная гипертония (5%) - когда высокое АД является одним из симптомов какого-то заболевания (например, почечная гипертония). Существует особая форма артериальной гипертонии, которую, с оговорками, можно отнести к возрастной: она называется "склеротическая артериальная гипертония". Как правило, данная форма гипертонии развивается у лиц старше 70-75 лет, довольно неплохо субъективно переносится, считается менее злокачественной (в плане осложнения инфарктом и инсультом). Ее специфическим признаком является большая разница между верхним и нижним давлением. Если при гипертонической болезни одновременно повышается и систолическое и диастолическое артериальное давление (например 200/110 мм.рт.ст), то при склеротической гипертонии диастолическое давление остается нормальным или низким, например - 200/70 мм.рт.ст. Резюме: если цифры вашего АД стабильно превышают значения 135/90 мм.рт.ст. - это является безусловным поводом обратиться к врачу.
Сердечная недостаточность
-
патологическое состояние, при котором сердце в единицу времени не может
перекачать в артериальное русло необходимый объем крови. В норме объем
крови притекаемый к сердцу равен оттекаемому (непрерывность потока). Нарушение
этого равновесия лежит в основе развития сердечной недостаточности (СН). Сердце
состоит из 4-х камер: правое и левое предсердия, правый и левый желудочек.
Несостоятельность хотя бы одной из них (когда приток и отток не эквивалентны) со
временем приводит к манифестации симптомов СН. Возможные причины сердечной
недостаточности: 1) патологическое функционирование клапанного аппарата сердца
(пороки сердца), 2) слабое сокращение камер(ы) сердца - кровь из них
выбрасывается в малом количестве (например, инфаркт миокарда, миокардит,
многолетняя мерцательная аритмия), 3)камер(ы)а сердца плохо расслабляются
(повышенная "жесткость" миокарда) - в "ригидную" камеру кровь притекает
недостаточно: например, диастолическая дисфункция левого желудочка при
гипертонической болезни, когда из-за жесткости левого желудочка кровь начинает
застаиваться в левом предсердии. Последний феномен легко понять на примере
присасывающего действия пипетки: представьте сжатую пипетку опущенную в воду, в
момент расжатия вода будет поступать в нее. Так вот если пипетка (сердце)
разожмется неполностью, воды (крови) поступит в нее (него) мало. 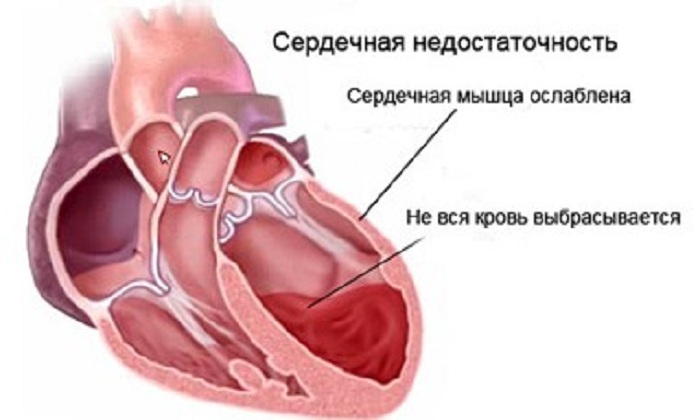
Самые ранние симптомы СН: немотивированная слабость и одышка при привычной физической нагрузке. Сочетание подобных симптомов, разумеется, встречается и при других заболеваний, но СН дебютирует именно с них. СН - это всегда следствие. Заболевания, чаще всего приводящие к развитию СН: ишемическая болезнь сердца, артериальная гипертония, врожденные или приобретенные пороки сердца, мерцательная аритмия. Указанные патологические состояние поражают все сердце или его отдельные камеры. Таким образом, чтобы недопустить развитие СН, необходимо лечить "заболевание-предтече". В запущенной стадии СН проявляется одышкой в покое (вплоть до удушья), отеками ног, выраженной слабостью, бледностью кожных покровов, синюшностью губ. СН неизбежно приводит к смерти. Другое дело, что ее адекватное лечение на ранних стадиях, приводит к многолетней ремиссии, позволяя жить десятилетия; в запущенных случаях, несмотря на самую современную и полноценную терапию, у пациента похоже есть не более 5 лет (это в лучшем случае). Пример из жизни: знаменитый советский актер Е.Леонов перенес несколько острых инфарктов миокарда, которые привели к развитию СН; в последние годы жизни он страдал от сильной одышки, выраженных отеков ног. Резюме: СН - это следствие какого-то органического заболевания сердца, и наличие ее симптомов в какой-то степени отражает далеко зашедшую стадию процесса; однако, лечение на ранней стадии позволяет существенно продлить жизнь больного.
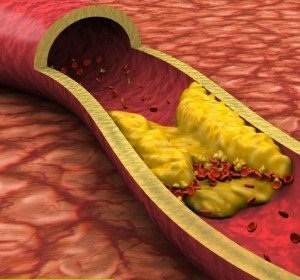
Гиперхолестеринемия - уровень холестерина крови превышающий нормальные значения - 5,5-6,5 ммоль/л. Это так называемый общий холестерин. Биохимически и лабораторно холестерин разделяют на "хороший" (ЛПВП) и "плохой" (ЛПНП, ЛПОНП). Уровень "хорошего" желательно иметь высоким, а "плохого" соответственно низким. В кардиологии зачастую используется другой термин: дислипидемия. Под дислипидемией понимают любое изменение нормального соотношения липидов крови, предрасполагающее к атеросклерозу. Например, общий холестерин нормальный, а его злокачественная фракция повышена, или уровень холестерина нормальный, а концентрация нейтрального жира (триглицериды) высокая. То есть дислипидемия более широкое понятие. Гиперхолестеринемия бывает первичная и вторичная. Первичная гиперхолестеринемия - генетически детерминированное заболевание; как любая врожденная патология встречается очень редко. Подозревать наследственную гиперхолестеринемию можно тогда, когда у человека беспричинно выявляется очень высокий холестерин крови, обычно - выше 11 ммоль/л и имеются ксантомы. Вторичная гиперхолестеринемия возникает на фоне приобретенного заболевания, одним из проявлений которого является повышенный холестерин. Самой распространенной причиной вторичной гиперхолестеринемии можно считать неправильное питание (пищевая липемия) - преобладание в пищевом рационе продуктов с высоким содержанием холестерина и насыщенных жирных кислот. Еще одной распространенной причиной вторичной гиперхолестеринемии является сахарный диабет. Некорректно леченный сахарный диабет всегда сопровождается дислипидемией, предрасполагая тем самым к атеросклерозу. Иногда мотивы вторичной гиперхолестеринемии не очевидны, в таком случае она чаще всего является проявлением неправильного образа жизни. Что принципиально отличает вторичную гиперхолестеринемию от первичной: она никогда не бывает слишком высокой (обычно концентрация общего холестерина не превышает 9-11 ммоль/л), и соответственно не так злокачественна (атерогенна). Остановимся на клиническом значении "холестериновой проблемы". Избыточная концентрация холестерина в крови с годами приводит к его отложению (по принципу градиента концентрации) в стенках тех артерий , которые испытывают наибольшее гемодинамическое воздействие (артерии сердца, аорта и ее крупные ветви) - со временем развивается атеросклероз этих сосудов.
 Для
кардиолога наибольший интерес представляет концентрация в крови "плохого"
холестерина - ЛПНП. Ситуации, когда уровень общего холестерина нормальный, а
"плохого" повышен - распространены и однозначно требуют внимания. В целом,
проблема гиперхолестеринемии, возможно, несколько преувеличена. Дошло до
того, что в последние годы некоторые исследователи допускают считать
нормальными значения общего холестерина до 7,5 ммоль/л. Подобные
разногласия порождены тем, что до сих пор непонятным остается тот факт,
почему лица имеющие высокий уровень холестерина, в том числе "плохого",
остаются клинически здоровы, доживая до старости; с другой стороны, есть
масса примеров, когда люди заболевают
атеросклерозом, имея нормальный холестерин крови. Резюме:
повышенный уровень холестерина крови - это всего лишь фактор риска
атеросклеротических заболеваний (инсульта и инфаркта миокарда);
манифестируют они или нет - предсказать невозможно; в совокупности с другими
факторами риска (например, курение, сахарный диабет, лишний вес), опасность
многократно возрастает. Цифры общего холестерина выше 8 ммоль/л требуют
однозначной коррекции (даже у молодых здоровых лиц), поскольку при такой
концентрации холестерина вероятность появления преждевременного
атеросклеротического заболевания крайне высока. В анализе крови "на
холестерин" прежде всего обращайте внимание на концентрацию ЛПНП и ЛПВП.
Для
кардиолога наибольший интерес представляет концентрация в крови "плохого"
холестерина - ЛПНП. Ситуации, когда уровень общего холестерина нормальный, а
"плохого" повышен - распространены и однозначно требуют внимания. В целом,
проблема гиперхолестеринемии, возможно, несколько преувеличена. Дошло до
того, что в последние годы некоторые исследователи допускают считать
нормальными значения общего холестерина до 7,5 ммоль/л. Подобные
разногласия порождены тем, что до сих пор непонятным остается тот факт,
почему лица имеющие высокий уровень холестерина, в том числе "плохого",
остаются клинически здоровы, доживая до старости; с другой стороны, есть
масса примеров, когда люди заболевают
атеросклерозом, имея нормальный холестерин крови. Резюме:
повышенный уровень холестерина крови - это всего лишь фактор риска
атеросклеротических заболеваний (инсульта и инфаркта миокарда);
манифестируют они или нет - предсказать невозможно; в совокупности с другими
факторами риска (например, курение, сахарный диабет, лишний вес), опасность
многократно возрастает. Цифры общего холестерина выше 8 ммоль/л требуют
однозначной коррекции (даже у молодых здоровых лиц), поскольку при такой
концентрации холестерина вероятность появления преждевременного
атеросклеротического заболевания крайне высока. В анализе крови "на
холестерин" прежде всего обращайте внимание на концентрацию ЛПНП и ЛПВП.
Атеросклероз
-
системное заболевание крупных артерий эластического типа, в основе которого
лежит отложение липидов (прежде всего холестерина) во внутренней стенке (интиме)
этих артерий. Существует несколько альтернативных, в какой-то степени
взаимоисключающих, теорий патогенеза атеросклероза. Однако главное, что их
объединяет: без холестерина нет атеросклероза. Поскольку атеросклероз признан
мультифокальным, полиэтиологическим заболеванием, то, говоря о его
происхождении, корректно использовать термин фактор риска,
а не причина. Факторы риска атеросклероза делятся на модифицируемые
(приобретенные) и немодифицируемые. К первым относятся те, которые можно
"упразднить": гиперхолестеринемия, курение, артериальная гипертония, сахарный
диабет и некоторые другие. Ко вторым - некорректируемые обстоятельства: возраст,
мужской пол, неблагоприятная наследственность. Наиболее логично атерогенез
объясняется
высоким уровнем холестерина
крови: избыток холестерина по градиенту концентрации поступает в
стенки артерий, где захватывается клетками; клетки, постепенно перегружаясь
холестерином, погибают; холестерин оказывается во внеклеточном пространстве,
где, накапливаясь, начинает формировать атеросклеротическую бляшку. Однако
гиперхолестеринемия встречается не более, чем в 2/3 случаев атеросклероза.
Значит другие факторы риска атеросклероза являются нелипидными. Наиболее
значимыми из них считаются курение и неконтролируемая артериальная гипертония. В
обеих случаях значительно увеличивается изнашиваемость артерий:
никотин активирует симпатическую нервную систему (объем крови с силой
выбрасывается из сердца, "травмируя" стенки артерий), а при артериальной
гипертонии стенки артерий оказываются под перманентным воздействием повышенного
кровяного давления, что также травмирует их. Избыточное гемодинамическое
воздействие на стенку артерий приводит к тому, что их внутренняя оболочка
начинает нуждаться в большом количестве строительного материала (холестерин,
один из обязательных компонентов биологической мембраны), который начинает
поступать в нее в избыточном количестве - а это уже, по сути, начало атерогенеза.
Что касается сахарного диабета - еще одного важнейшего фактора риска
атеросклероза - то следует признать, что практически всегда он сопровождается
дислипидемией. Поэтому, вероятно, базовым механизмом атерогенеза при сахарной
диабете является отложение липидов в стенке артерий по принципу градиента
концентрации. Раньше всего атеросклерозу подвергается аорта, ее ветви, места
естественных изгибов артерий и бифуркаций (деления) - то есть крупные сосуды,
чья стенка испытывает наибольшие гемодинамические воздействия, и где происходит
завихрение, турбулентный поток крови. Сформированная атеросклеротическая бляшка
может иметь эксцентрическую или концентрическую конфигурацию. Эксцентрическая
бляшка уплощена, не влияет на кровоток и поэтому клинически бессимптомна.
Концентрическая бляшка сужает просвет артерии. Гемодинамически значимым
считается сужение не менее чем на 70%. Под гемодинамической значимостью стеноза
понимается такое сужение, когда возрастание нагрузки на орган, питаемый данной
артерией, сопровождается его ишемией, вследствие снижения кровотока. В далеко
зашедшей стадии атеросклероза просвет артерии полностью облитерируется
(перекрывается) - кровоток по такому сосуду
прекращается.
Таким образом, главным патофизиологическим феноменом атеросклероза является ишемия или, по другому, нехватка крови (кислорода) в той области, которая кровоснабжается данной артерией. Субъективные проявления феномена ишемии, зависят от того, какой орган страдает. Например, в сердечной мышце, ишемия проявляется в основном болью в грудной клетке (стенокардия, острый инфаркт миокарда); в головном мозге - головокружением, слабостью, нарушением речи и прочее; в артериях нижних конечностей - перемежающей хромотой. С одной стороны, атеросклероз прочно ассоциирован с общим старением организма, с другой стороны, атеросклерозом могут болеть лица любого возраста. В последнем случае он, как правило, развивается при наличии факторов риска. Еще раз повторю первостепенные из них: гиперхолестеринемия, курение, неконтролируемая артериальная гипертония, сахарный диабет, ожирение. Кроме того, раннему атеросклерозу подвержены лица, с контролирующим типом поведения, например, начальники, и субъекты испытывающие хронический дефицит положительных эмоций ("окостенение" артерий). Типичный облик "коронарной" личности: профессионал, предъявляющий высокие требования к окружающим при недостаточно эффективном контроле по субъективным или объективным причинам, что вызывает ощущение внутренней неудовлетворенности, раздражения. У пожилых людей, которые, вероятно, в силу экзистенциальных причин постепенно перестают радоваться жизни, атеросклероз может развиваться стремительно. Наконец, нельзя забывать о наследственной предрасположенности к атеросклерозу; в качестве примера - ранее заболевание (до 50 лет) близким родственником инфарктом миокарда. В таком случае сама наследственность является фактором риска. Наиболее известные атеросклеротические заболевания или их клинические формы: стенокардия, ишемическая болезнь сердца, инсульт, перемежающая хромота. Основной "патофизиологической драмой" атеросклероза является надрыв бляшки и формирование в этом месте тромба, который за секунды может полностью перекрыть просвет артерии. Именно по такому сценарию развиваются большинство инфарктов и инсультов. Причем "надорваться" может бляшка небольших размеров, в том числе гемодинамически незначимая, эксцентрическая.
Клиническое коварство атеросклероза заключается в том, что он долгие годы может протекать бессимптомно, а затем хронологически непредсказуемо, без предвестником приводить к жизнеугрожающему состоянию: инфаркт миокарда или инсульт. В связи с чем, крайне важно заниматься первичной профилактикой атеросклероза, которая сводится к здоровому образу жизни: не переедать, регулярно нагружать себя физически, следить за своим весом, не курить, контролировать артериальное давление, избегать стрессовой работы. Вне зависимости от пола первым всегда развивается атеросклероз аорты - он бессимптомен. Затем у мужчин атеросклерозом поражаются коронарные артерии; до поры до времени он может быть бессимптомным, но впоследствии обязательно осложняется стенокардией или инфарктом миокарда. У женщин вслед за атеросклерозом аорты чаще развивается атеросклероз артерий мозга - возникает риск развития дисциркуляторной энцефалопатии, инсульта; впрочем, мозговой атеросклероз также долгие годы может протекать бессимптомно. У мужчин вслед за коронарным атеросклерозом поражаются мозговые артерии (риск инсульта) или артерии подвздошно-бедренного сегмента (перемежающая хромота) - примерно с одинаковой вероятностью. У женщин после мозгового атеросклероза поражаются коронарные артерии и развивается ИБС. Перемежающая хромота для женщин не характерна.
Перед назначением статинотерапии необходимо оценить генез атеросклероза: липидный или нелипидный. При липидном атеросклерозе терапия статинами является обязательной, она - высокоэффективна. При нелипидном атеросклерозе протективный эффект статинотерапии сомнительный; в таком случае упор следует сделать на борьбу с нелипидными факторами риска атеросклероза: курение, артериальная гипертония и т.д.
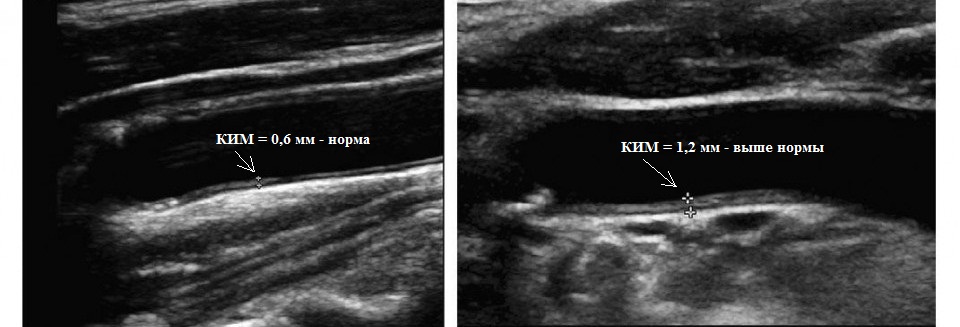
Самым ранним клиническим маркером латентного (бессимптомного) атеросклероза является увеличение толщина комплекса интима-медиа (КИМ): суммарная толщина внутреннего и среднего слоя артерии. Этот параметр определяется, главным образом, при УЗИ сонных артерий. Безотносительно к возрасту он не должен превышать 1 мм. Однако все же корректнее нормировать величину КИМ исходя из возраста и пола: для мужчин до 40 лет КИМ должен быть не более 0,7 мм, от 40 до 50 лет - 0,8 мм, старше 50 лет - 0,9 мм, для женщин до 45 лет - 0,7 мм, от 45 до 60 лет - 0,8 мм, старше 60 лет - 0,9 мм. Патологического значения толщины КИМ ассоциировано с накоплением в стенке артерии атерогенных липидов. Выявление данного факта позволяет принять превентивные антиатерогенные меры.
Инфаркт миокарда - клиническая форма ишемической болезни сердца, характеризующаяся развитием некроза (омертвения) участка сердечной мышцы. В абсолютном большинстве случаев инфаркт миокарда (ИМ) развивается вследствие возникновения острого тромбоза сердечной артерии, что влечет за собой полное прекращение по ней кровотока:

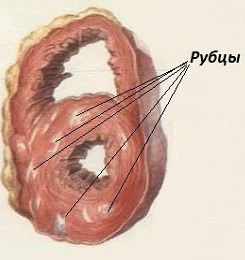
Самым ранним и частым симптомом ИМ является сильная, часто нестерпимая, боль за грудиной, сопровождающаяся выраженной потливостью. Другие возможные ощущения (одышка, слабость) появляются либо совместно с болью, либо несколько позже ее. ИМ - грозное осложнение ишемической болезни сердца: среди причин смертности лиц средних и старших возрастных групп, это заболевание, наряду с инсультами и онкопатологией, занимает ведущее место. Течение заболевания вариабельно: ИМ может привести к смерти, несмотря на оказание самой быстрой и полной медицинской помощь; с другой стороны, некоторые люди переносят инфаркт "на ногах" - в такой ситуации его диагностируют ретроспективно. Все же в большинстве случаев только экстренная медицинская помощь способна уберечь человека если не от смерти, то от серьезных осложнений (ближайших и отдаленных) инфаркта миокарда. Инфаркт миокарда можно перенести несколько раз, некоторые умирают от первого. Перенесенный ИМ является серьезным звонком, сигнализирующим о том, что в жизни человека есть какая-то причина (фактор риска), спровоцировавшая столь грозное заболевание - например, курение. Если такой больной бросает курить, он в десятки раз снижает риск повторного (всегда, как минимум, инвалидизирующего) инфаркта миокарда, и тем самым дает себе шанс на долгую жизнь. Существует целый ряд других факторов риска, ассоциирующихся с ранним развитием ИМ и укладывающихся в идиому под названием "неправильный образ жизни". Поэтому, если вас постигло это заболевание, надо задать вопрос: почему заболел именно я? В глубокой старости ИМ чаще всего является фатальным, отражая естественные процессы старения и умирания организма.
За годы работы в инфарктном отделение я повидал сотни больных с острым инфарктом миокарда. Для себя (негласно) инфаркт миокарда я разделяю на старческий и нестарческий. "Старческий инфаркт" возникает у лиц соответствующего возраста и как бы без видимых причин (так думают родственники больного). Старость понятие относительное, поскольку один человек может в 60 лет выглядеть на 80 и наоборот. Люди, которые выглядят заскорузлыми внешне, как правило, стары и изнутри (атеросклероз сосудов); они могут заболеть острым инфарктом миокарда просто так... потому что возраст подошел опасный. В таком случае инфаркт миокарда, является одним из драматичных проявлений старения, общего изнашивания сосудов, увядания организма. Разумеется, больные со "старческим" инфарктом могут благополучно его пережить, выписаться из больницы и прожить еще немало лет. Суть в другом: подобный инфаркт носит только возрастной оттенок. Я акцентирую на этом внимание, потому что нередко приходиться слышать вопросы от больного или от его родственников, мол, почему заболел, "ведь не пил, не курил, по девкам не ходил"! Я им и отвечаю, что это просто старость. Именно так к нам в отделение попадают совершенно здоровые старики, которые "ничем и никогда не болели". Условная возрастная граница, когда инфаркт скорее "старческий": от 70 лет в независимости от пола. Совершенно иной философский посыл имеет "нестарческий инфаркт". Инфарктом миокарда можно заболеть в любом возрасте; например, в своей практике я встречал 26-летнего пациента с инфарктом. Практически ежедневно к нам в отделение поступают лица 40-50 лет с сердечным приступом. Такие относительно молодые больные практически всегда имеют какую-то видимую причину столь раннего возникновения заболевания. Каждый "нестарческий" инфаркт миокарда развивается на фоне фактора риска, который для конкретного пациента становиться причиной заболевания. Главные факторы риска "нестарческого" инфаркта миокарда: большой стаж курения (от 10-15 лет), многолетняя неконтролируемая артериальная гипертония, высокий уровень холестерина крови (который часто сопряжен с избыточным весом, руководящей должностью на работе, холеричным темпераментом), хронический стресс и некорригируемый сахарный диабет. Каждый из названных факторов риска может в разы ускорять развитие атеросклероза, а значит "приближать человека к беде". "Нестарческий" инфаркт миокарда - это своеобразный посыл больному, от том, что его образ жизни несовместим с долголетием. Поэтому необходимо устранить из своей жизни факторы риска - только в таком случае второго инфаркта может не быть. Если же фактор риска не устранен, обязательно(!) будет повторный инфаркт, скорее смертельный. В реальной жизни знаю больных, которые переносили инфаркт еще в конце 80-х, однако, "взявшись за ум", они благоденствуют и по сей день. Так что, многое в руках человека.
Ишемическая болезнь сердца (ИБС) - самое распространенное заболевание сердца и самая частая причина сердечной смерти. В основе ИБС лежит атеросклероз артерий сердца. Многие годы заболевание может протекать бессимптомно и манифестировать, например, с острого инфаркта миокарда. Однако, чаще ИБС дебютирует со стенокардии и ею многие годы ограничивается.
 Возможны
другие варианты начала ИБС: внезапная смерть, аритмии, пароксизмальная
одышка - но это исключение. В нашей стране наблюдается гипердиагностика ИБС:
едва ли не любая боль за грудиной или в области сердца трактуется, как
стенокардия. Вместе с тем, учитывая, что постановка такого грозного диагноза
является само по себе ответственной задачей, необходимы весомые клинические
аргументы для доказательства ИБС. В идеале диагностический поиск должен
проводиться в порядке усложнения исследования и повышения его
чувствительности. 1. Опрос больного: стенокардия - диагноз клинический и с
вероятностью 90-95% устанавливается с помощью обычного детального
опроса. 2. При сомнительных болях в области сердца пациенту необходимо
провести тест с физической нагрузкой с одновременной регистрацией ЭКГ (тредмил-тест,
велоэргометрия) - он может выявить корреляцию между нагрузкой и
ишемическими изменениями на ЭКГ. 3. Если результаты теста отрицательные или
неоднозначные, то целесообразно закончить диагностический поиск, проведением
коронарографии. Данная диагностическая методика позволяет визуализировать в
артериях сердца гемодинамически значимые сужения и с вероятностью 99%
подтвердить или опровергнуть стенокардию (ИБС, атеросклероз сердечных
артерий). К сожалению, в российской медицине первые 2 этапа часто проводятся
некорректно и приходится сталкиваться с ситуацией, когда у больного имеются
заведомо нестенокардитические боли, однако его отправляют на коронарографию
(инвазивная диагностика с определенным процентом серьезных осложнений), при
которой стенозов в сердечных артериях не находят.
Возможны
другие варианты начала ИБС: внезапная смерть, аритмии, пароксизмальная
одышка - но это исключение. В нашей стране наблюдается гипердиагностика ИБС:
едва ли не любая боль за грудиной или в области сердца трактуется, как
стенокардия. Вместе с тем, учитывая, что постановка такого грозного диагноза
является само по себе ответственной задачей, необходимы весомые клинические
аргументы для доказательства ИБС. В идеале диагностический поиск должен
проводиться в порядке усложнения исследования и повышения его
чувствительности. 1. Опрос больного: стенокардия - диагноз клинический и с
вероятностью 90-95% устанавливается с помощью обычного детального
опроса. 2. При сомнительных болях в области сердца пациенту необходимо
провести тест с физической нагрузкой с одновременной регистрацией ЭКГ (тредмил-тест,
велоэргометрия) - он может выявить корреляцию между нагрузкой и
ишемическими изменениями на ЭКГ. 3. Если результаты теста отрицательные или
неоднозначные, то целесообразно закончить диагностический поиск, проведением
коронарографии. Данная диагностическая методика позволяет визуализировать в
артериях сердца гемодинамически значимые сужения и с вероятностью 99%
подтвердить или опровергнуть стенокардию (ИБС, атеросклероз сердечных
артерий). К сожалению, в российской медицине первые 2 этапа часто проводятся
некорректно и приходится сталкиваться с ситуацией, когда у больного имеются
заведомо нестенокардитические боли, однако его отправляют на коронарографию
(инвазивная диагностика с определенным процентом серьезных осложнений), при
которой стенозов в сердечных артериях не находят.
Коронарография - диагностическая процедура, которая заключается во введении в артерии сердца контрастного вещества, что под контролем рентгеноскопии позволяет оценить их проходимость, выявить сужения.
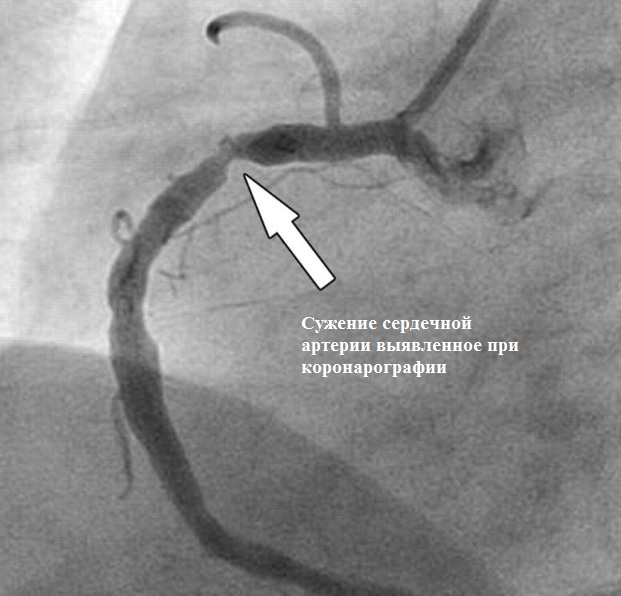 Коронарография
инвазивная манипуляция: осуществляется прокол
одной из крупных периферических артерий (чаще бедренной или лучевой), через
которую проводник доводят до сердца. Как любая инвазивная методика,
коронарография имеет свой процент осложнений, в том числе летальных; поэтому
она всегда сопряжена с некоторым риском и требует обязательной
госпитализации больного в стационар минимум на 1-2 дня. Коронарография
безболезненна и проводится без наркоза под местной анестезией (место
пункции). В опытных руках осложнения при ее выполнении составляют менее 1%.
Коронарография является золотым стандартом диагностики
ишемической болезни сердца; другое дело что ее
проведение должно быть оправдано с клинической точки зрения. Так встречаются
ситуации, когда боли в грудной клетки явно нестенокардитические, однако
врач, видимо от своей профессиональной беспомощности, отправляет пациента
на коронарографию. Все же роль ее в современной кардиологии очень велика:
порой только коронарография позволяет закончить длительный диагностический
поиск.
Коронарография
инвазивная манипуляция: осуществляется прокол
одной из крупных периферических артерий (чаще бедренной или лучевой), через
которую проводник доводят до сердца. Как любая инвазивная методика,
коронарография имеет свой процент осложнений, в том числе летальных; поэтому
она всегда сопряжена с некоторым риском и требует обязательной
госпитализации больного в стационар минимум на 1-2 дня. Коронарография
безболезненна и проводится без наркоза под местной анестезией (место
пункции). В опытных руках осложнения при ее выполнении составляют менее 1%.
Коронарография является золотым стандартом диагностики
ишемической болезни сердца; другое дело что ее
проведение должно быть оправдано с клинической точки зрения. Так встречаются
ситуации, когда боли в грудной клетки явно нестенокардитические, однако
врач, видимо от своей профессиональной беспомощности, отправляет пациента
на коронарографию. Все же роль ее в современной кардиологии очень велика:
порой только коронарография позволяет закончить длительный диагностический
поиск.
Стентирование - применительно к кардиологии: современное лечение ИБС, которое заключается в установке тонкой, сетчатой металлической трубочки в участок сердечной артерии, суженной атеросклеротической бляшкой. Данная методика относится к малоинвазивным - она не подразумевает общего наркоза и вскрытия грудной клетки. Манипуляция осуществляется через прокол одной из периферических артерий (лучевой или бедренной); вводится специальный проводник, с помощью которого стент (под контролем рентгеноскопии) "доставляется" к месту назначения; последний этап - раздутие стента баллоном; итог: суженный участок артерии вновь проходим. Процедура выполняется под местной анестезией (анестезируется место пункции и, как правило, в\в вводится седативный препарат). Со слов пациентов, данная операция абсолютно безболезненна.
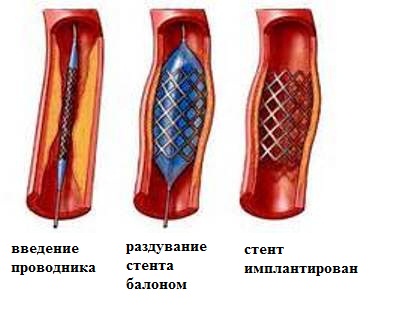
 Стент
является высокотромбогенным и без приема специальных лекарств неминуемо
затромбируется. Поэтому после стентирования в течение минимум 1 года больной
должен принимать
антиагрегантный препарат, который будет препятствовать
тромбированию стента. За текущий период стент изнутри обрастает эндотелием
(естественная оболочка артерии) и перестает быть тромбогенным. Пренебрежение
приемом этих лекарств чревато развитием тромбоза стента (острая окклюзия
артерии), приводящего к
инфаркту миокарда.
Стент
является высокотромбогенным и без приема специальных лекарств неминуемо
затромбируется. Поэтому после стентирования в течение минимум 1 года больной
должен принимать
антиагрегантный препарат, который будет препятствовать
тромбированию стента. За текущий период стент изнутри обрастает эндотелием
(естественная оболочка артерии) и перестает быть тромбогенным. Пренебрежение
приемом этих лекарств чревато развитием тромбоза стента (острая окклюзия
артерии), приводящего к
инфаркту миокарда.
Аспирин (ацетилсалициловая кислота) - лекарственный препарат, обладающий противовоспалительным, обезболивающим, жаропонижающим эффектами. В середине прошлого столетия было установлено, что кроме всего прочего ацетилсалициловая кислота препятствует агрегации (слипанию) тромбоцитов и образованию артериальных тромбов. Поэтому основная точка приложения аспирина в кардиологии - профилактика тромбоза в артериях сердца - защита от жизнеугрожающего осложнения ИБС - инфаркта миокарда. "Аспириновый бум" продолжается до сих пор. В многочисленных исследованиях было доказано, что регулярный прием ацетилсалициловой кислоты в разы снижает риск развития инфаркта миокарда и вообще сосудистой смертности. В настоящее время постановка диагноза ИБС, стенокардия автоматически означает пожизненное назначение аспирина. Всем мужчинам старше 50 лет и женщинам старше 60 лет рекомендуется ежедневный прием аспирина даже при отсутствии заболевания, поскольку и у этой категории лиц был доказан его протективный эффект (снижение смертности от инсультов и инфарктов). Однако ацетилсалициловая кислота не является панацеей от тромбообразования, поскольку тромботический каскад - процесс многофакторный; кроме того, есть субъекты нечувствительные к аспирину - примерно у 5-10% людей он не вызывает антиагрегантного эффекта. Настоящая медицинская действительность (во всяком случае в Хабаровске) не позволяет провести лабораторную диагностику на наличие индивидуальной чувствительности (антитромбоцитарного эффекта) к аспирину, поэтому при наличии показаний он назначается всем в 100% случаев. Сейчас в почете разнообразные формы аспирина в "облатке", снижающие его "ульцерогенный" эффект. Я люблю назначать Кардиомагнил (аспирин+щелочь).
Плавикс (Клопидогрель, Зилт и др.) - лекарственный препарат из группы антиагрегантов. Является достойным дополнением (не альтернативой!) аспирина в плане профилактики тромбообразования в артериях. Имеет и свою индивидуальную нишу применения. В основном плавикс назначается после стентирования коронарных артерий с целью предотвращения тромбоза стента (вместе с аспирином); вторая распространенная ситуация при которой показан плавикс - индивидуальная непереносимость аспирина или нечувствительность к нему (последнее обстоятельство труднодоказуемо). После стентирования плавикс предписывается минимум на год; за это время стент обрастает изнутри естественной тканью артерии и перестает быть тромбогенным. Актуальной является проблема резистентности (отсутствие антитромбоцитарного эффекта) к плавиксу - около 5% людей к нему нечувствительны. Плавикс можно не применять 1) при стабильном течении ИБС в отсутствии стентирования, 2) спустя год после стентирования. Все выше сказанное распространяется и на ультрасовременный антиагрегант Брилинта; это улучшенный аналог плавикса - к нему не наблюдается резистентность. Однако, он дороже.
Кордарон - современный, мощный антиаритмический препарат. По силе антиаритмического эффекта превосходит все другие лекарства этой группы. Эффективно подавляет экстрасистолию, различные тахиаритмии. Но!... Обладает целым рядом отдаленных побочных эффектов, которые развиваются спустя 5-10 лет регулярного приема кордарона. Следует выделить основные из них: поражение щитовидной железы, склеротические процессы в легких, нарушение зрение, пигментация кожи. Повторюсь, они развиваются через многие годы, но по сути являются необратимыми. Токсичность кордарона определяется наличием в его составе молекулы йода: с одной таблеткой мы получаем количество йода в десятки раз превосходящее его суточную потребность. Кордароновые осложнения не несут непосредственной угрозы, поэтому если его прием необходим (например, по жизненным показаниям), то возникшие побочные эффекты медикаментозно корректируются, а лекарство употребляется дальше. Назначая кордарон, врач всегда должен взвешивать риск и пользу от его приема. Я его применяю в следующих клинических ситуациях: 1) жизнеугрожающие желудочковые нарушения ритма (в такой ситуации практически эффективен только он один) - ситуация пан или пропал, 2) кратковременно перед предполагаемой радикальной антиаритмической операции на сердце (например, перед радиочастотной аблацией при мерцательной аритмии или синдроме WPW) - длительность приема от нескольких месяцев до года, 3) для оказания экстренной помощи в госпитальных условиях. Например, для купирования приступа мерцательной аритмии кордарон вводится внутривенно, 4) пожилым людям при симптоматичных аритмиях (старше 70-80 лет). В последнем случае польза заведомо превышает риск. Статистически лица данной возрастной группы проживают не более 10-15 лет. Назначая им кордарон мы обеспечиваем чудодейственное исцеление от тягостно переносимой аритмии, а до его побочных эффектов пациенты скорее всего не доживают, умирая от естественных причин. Нередко!... в клинической практике встречаешься с ситуациями, когда кордарон длительно назначается, например, при безобидной желудочковой экстрасистолии. На мой взгляд, это абсолютно недопустимо! Кордарон - токсичный препарат, который должен назначаться, повторюсь, по строгим показаниям.
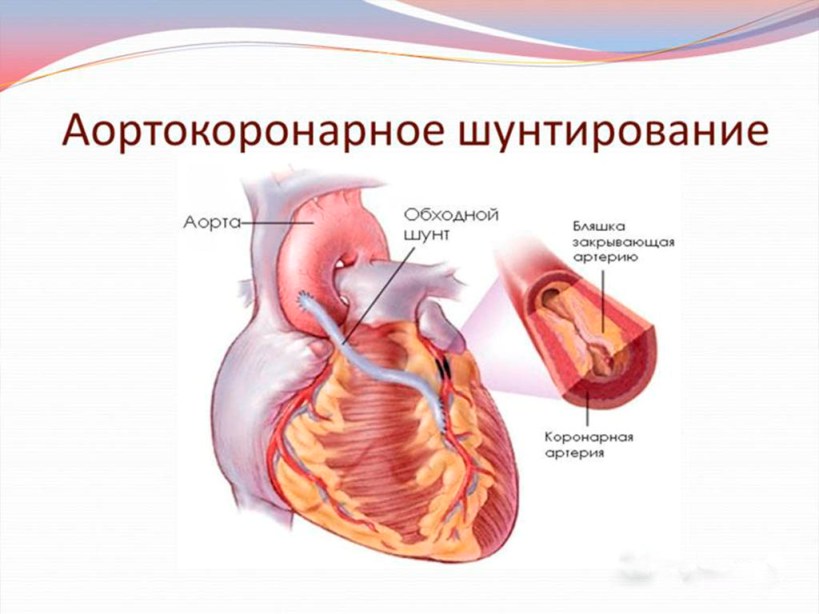
Аортокоронарное шунтирование (АКШ) - хирургическое лечение ИБС, заключающееся в формировании обходных сосудистых путей (шунтов) в местах, где локализуются атеросклеротические бляшки. Представьте себе сердечную артерию, состоящую из последовательных отделов А, B, С; кровь идет из А через В к С. Отдел В засорился (закупорился атеросклеротической бляшкой). Из поверхностных вен нижних конечностей пациента (вырезают одну-две вены) создают шунт, один конец которого фиксирован к отделу А, другой к С; в итоге ток крови идет по шунту от А к С в обход В. АКШ - серьезная полостная операция, сопряженная с общим наркозом, вскрытием грудной клетки, искусственным кровообращением и прочими атрибутами кардиохирургической интервенции. В настоящее время, достойной альтернативой АКШ является операция стентирования. Однако, есть клинические ситуации, когда пациенту могут предложить только АКШ - как правило, это запущенные случаи с множественными поражениями коронарных артерий, когда стентирование невозможно или опасно.
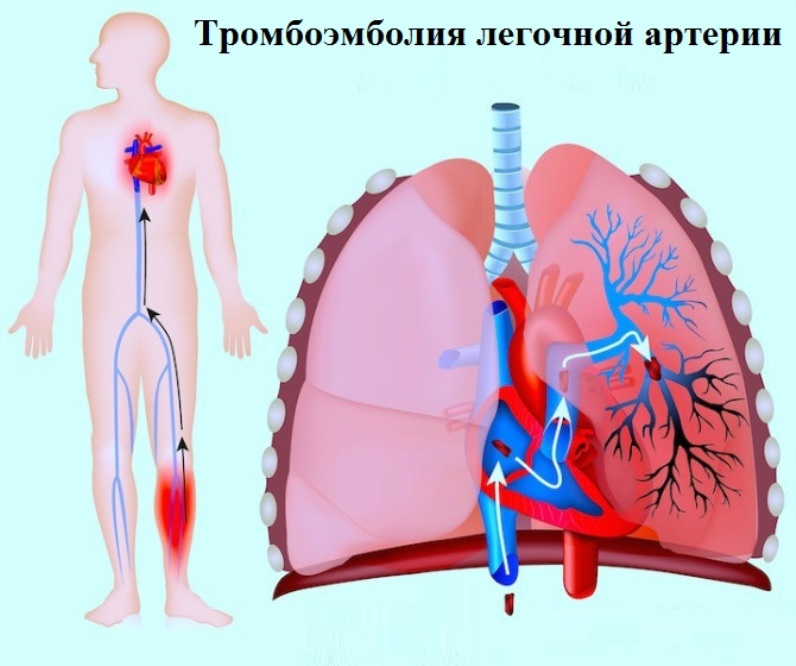
Тромбоэмболия легочной артерии (ТЭЛА) - жизнеугрожающее состояние, при котором в ветви легочной артерии током крови заносятся тромботические массы, обтурирующие (перекрывающие) просвет сосудов. Это приводит к резкому снижению кровотока через легкие и симметричному уменьшению системного кровотока; значительно падает оксигенация крови. Кардинальным симптомом ТЭЛА является внезапная, немотивированная одышка в покое; либо одышка появляется при ходьбе на небольшие расстояния, которые раньше человек беспроблемно преодолевал. Представьте, что вы пробежали спринт; в этом случае появление одышки кажется таким же естественным, как и ее отсутствие в покое. Так вот у больных с ТЭЛА одышка такая, как будто они "вагоны разгружали", хотя на самом деле они не делали ничего или почти ничего. В зависимости от величины тромбоэмболов клиника заболевания варьирует от едва ощутимой одышки, до внезапной резчайшей одышки, заканчивающейся быстрой смертью. В клинической практике чаще всего приходиться сталкиваться со случаями субмассивной ТЭЛА, когда тромбоз легочных артерий значительный, но своевременное оказание медицинской помощи позволяет спасти жизнь больного. Закономерен вопрос: откуда берутся эти тромбы? В 90% случаев тромбы формируются в крупных венах нижних конечностей; в остальных - в венах малого таза. Единственным местом где может "осесть" оторвавшийся тромб - ветви легочной артерии. Факторы риска тромбоза вен и ТЭЛА: женский пол, избыточная масса тела, сидячий образ жизни, прием оральных контрацептивов, пожилой возраст, длительная иммобилизация (например, после перелома ноги), онкологические заболевания, курение. Сочетание нескольких факторов увеличивает риск заболевания. По моим наблюдениям пациентов с ТЭЛА, поступающих в кардиологический стационар, можно разделить на 3 клинико-социальные группы: 1) лица старческого возраста (в таком случае процессы неконтролируемого тромобообразования в венах связаны с общим старением организма); 2) пациенты, вынужденные длительно (недели, месяцы) находится на постельном режиме - например, после перелома костей таза, ног, позвоночника; 3) женщины среднего возраста - 40 - 50(60) лет - имеющие факторы риска: избыточный вес, курение, сидячий образ жизни, прием оральных контрацептивов (достаточно сочетание 1-2 факторов риска, чтобы в разы увеличить риск заболеть ТЭЛА). Пример из жизни: актриса Л.М.Гурченко после перелома ноги длительно находилась в вынужденном положении лежа; тромбоз вен нижних конечностей осложнился массивной ТЭЛА и смертью.
Пороки сердца - разнородная группа заболеваний сердца, которых объединяет наличие макроскопических изменений в камерах и(или) клапанах сердца, приводящие к нарушениям внутрисердечной и системной гемодинамики. Пороки сердца делятся на врожденные и приобретенные. Врожденные пороки обусловлены аномалией внутриутробного развития плода. Классическим примером такого порока является дефект межпредсердной перегородки, когда между предсердиями имеется сообщение, в норме присутствующее только у плода. В соответствии с принципом градиента давления возникает дополнительный внутрисердечный поток крови (слева направо), что приводит к перегрузки правых камер сердца. В зависимости от размера дефекта порок может проявиться уже с раннего возраста, либо клинически манифестировать во взрослом состоянии. Так нередки случаи, когда порок является случайной находкой, например, у физически крепкого мужчины средних лет при плановом УЗИ сердца. Существует несколько десятков врожденных пороков сердца; для желающих подробно ознакомиться с ними рекомендую обратиться к специальной литературе. Приобретенные пороки сердца - это следствие какого-то заболевания, перенесенного уже после рождения. В настоящее время имеет смысл говорить о двух разновидностях таких пороков: ревматические и сенильные. Первые развиваются на фоне рецидивирующих ангин (как правило в подростковом возрасте), которые осложняются системным аутоиммунным воспалением соединительной ткани, прежде всего клапанов сердца (ревматизм); вторые являются классическим примером возрастного (инволютивного) поражения сердечного клапанного аппарата вследствие отложения в них солей кальция. Независимо от причины при приобретенных пороках сердца всегда изолировано поражаются клапаны (один или несколько); возникает либо их деформация и разрушение с развитием недостаточности, либо сращение клапанных створок с развитием стеноза. При недостаточности клапан пропускает кровь обратно в ту камеру из которой кровь в него притекла; при стенозе возникает препятствие для оттока крови. Единственным и неотвратимым следствием порока сердца является развитие сердечной недостаточности. Самый ранний симптом заболевания - одышка, появляющаяся и нарастающая постепенно, исподволь. В настоящее время ревматические пороки сердца успешно корригируются хирургическим путем; успех в лечении сенильных пороков зависит от возраста больного - у лиц старческого возраста риск не перенести сложную полостную операцию очень высок, поэтому им нередко показано только лекарственное лечение сердечной недостаточности. Приобретенные пороки сердца могут длительное время (10-20 лет) протекать бессимптомно и выявляться случайно, например, при прохождении медкомиссии: врач выслушивает шум в сердце. Диагностирование порока не означает проведение немедленной хирургической операции. Такой пациент должен находиться на постоянном учете у кардиолога. Только когда порок сердца манифестирует симптомами сердечной недостаточности (а это рано или поздно происходит), ставиться вопрос о его хирургической коррекции; если операцию своевременно не сделать, больной проживает не более 5-7 лет от момента появления первых симптомов.

Артериальная гипотония - в противоположность артериальной гипертонии, представляет собой синдром пониженного артериального давления. Артериальная гипотония может быть первичной и вторичной. В последнем случае она является одним из симптомов какого-то заболевания: например, сердечной недостаточности, гипокортицизма и др. Нас больше интересует первичная (беспричинная) артериальная гипотония, имеющая неофициальное название: гипотоническая болезнь. Критерии диагноза: 1) стабильно низкое артериальное давление (ниже 100/60 мм. рт. ст.), 2) неизвестная этиология заболевания, 3) манифестация его в юношеском возрасте (14-18 лет), 4) наличие определенной симптоматики. Сочетание всех критериев является обязательным. Так, например, пониженное АД при отсутствии симптомов болезнью не является. Жалобы пациентов с гипотонической болезнью неспецифичны: слабость (кардинальный симптом!), плохая переносимость физических нагрузок, эпизоды предобморочных состояний, периодические головокружения. В целом это относительно редкая проблема; еще реже она является поводом для обращения к врачу. Молодые женщины представляют собой основной контингент таких больных. У пациентов с гипотонической болезнью имеется вегетативный дисбаланс, когда регуляторные механизмы контролирующие артериальное давление недостаточно его повышают или, иногда, даже парадоксальным образом понижают. Лечение заболевания представляет определенные трудности, поскольку лекарств в таблетированной форме повышающих артериальное давление нет (во всяком случае в Хабаровске). Поэтому основным в лечении являются немедикаментозные средства: 1) пищевой рацион с повышенным содержанием соли, 2) объем употребляемой жидкости должен быть не менее 2 литров в сутки, 3) обязательная регулярная (желательно ежедневная) физическая активность аэробного характера (бег трусцой, ходьба, плавание, йога и т.п.), 4) не возбраняется прием напитков с повышенным содержанием кофеина (естественный кардиотоник): кофе, крепкий чай. В целом прогноз при гипотонической болезни благоприятный: она способна ухудшить качество жизни, но не ассоциируется с повышенной смертностью. Нередко гипотоническая болезнь спонтанно разрешается к 30-35 годам - артериальное давление становится нормальным и происходит фактическое выздоровление.
ЭКГ (электрокардиография) - метод поверхностной регистрации электрической активности сердца. Сердце является генератором электрического тока, который создает вокруг него электрическое поле. С помощью электродов на поверхности тела можно регистрировать разность потенциалов в каждый момент времени работы сердца и посредством специальной аппаратуры преобразовать это в кривую. Сердце находится в постоянном движении благодаря непрерывным внутриклеточным процессам деполяризации (генерация тока) и реполяризации (разрядка); непрерывность электромеханической работы сердца обусловливает то, что направление тока (электродвижущей силы) постоянно меняется по стандартной траектории. Регистрация изменения направления электродвижущей силы и приводит к формированию характерных зубцов на ЭКГ. Любая значимая патология сердца приводит к локальным или диффузным нарушениям электрических процессов, которые могут отразиться на ЭКГ - происходит отклонение направления электродвижущей силы от стандартной траектории. В кардиологии диагностическая значимость ЭКГ может быть абсолютно разной. Условно разделим ее на 3 категории: 1) роль ЭКГ исключительна и первостепенна - распространяется на все аритмические заболевания и синдромы; 2) роль ЭКГ очень важна, но существуют альтернативные методы диагностики - инфаркт миокарда, ТЭЛА, перикардит; 3) роль ЭКГ только вспомогательная - кардиомиопатии, гипертоническая болезнь, кардионевроз, миокардиодистрофии, гипертрофии, пороки сердца и др.
Пролапс митрального клапана (ПМК) - провисание створок митрального клапана в полость левого предсердия в момент сокращения левого желудочка.
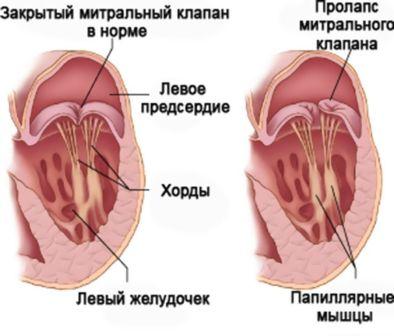 Одна из
самых распространенных врожденных аномалий развития сердца. От порока
отличается тем, что в подавляющем большинстве случаев ПМК не приводит к
нарушениям гемодинамики, не представляя никакой угрозы для жизни. ПМК
является одним из проявлений синдрома дисплазии соединительной ткани.
В основе этого синдрома лежит непрочность, слабость соединительной ткани,
которая присутствует практически в любом органе, в том числе в структуре
митрального клапана. Причина указанного синдрома - патология внутриутробного
развития, когда "что-то пошло не так". В зависимости от глубины
провисания створок ПМК бывает трех степеней. На пролапс 1 степени приходится
свыше 90% случаев и практически всегда он гемодинамически незначим.
Клиническая (гемодинамическая) значимость ПМК определяется тяжестью
митральной регургитации (недостаточности). Чем выше степень пролапса, тем
большее количество крови регургитирует (возвращается) в левое предсердие,
что соответственно повышает клиническую значимость этой аномалии. Наблюдения
требуют пациенты: 1) с пролапсом 2 или 3 степени; 2) если створки
митрального клапана миксоматозно изменены; 3) если ПМК сочетается с
множественными дополнительными хордами в левом желудочке. Обозначенная
категория лиц находится в группе риска в плане формирования в будущем
развернутой болезни сердца (порок сердца или аритмический синдром). Лица с
ПМК 1 степени и без дополнительных аномалий в диспансеризации не нуждаются -
они здоровы.
УЗИ сердца
позволяет визуализировать ПМК, оценить его степень и гемодинамическую
значимость.
Одна из
самых распространенных врожденных аномалий развития сердца. От порока
отличается тем, что в подавляющем большинстве случаев ПМК не приводит к
нарушениям гемодинамики, не представляя никакой угрозы для жизни. ПМК
является одним из проявлений синдрома дисплазии соединительной ткани.
В основе этого синдрома лежит непрочность, слабость соединительной ткани,
которая присутствует практически в любом органе, в том числе в структуре
митрального клапана. Причина указанного синдрома - патология внутриутробного
развития, когда "что-то пошло не так". В зависимости от глубины
провисания створок ПМК бывает трех степеней. На пролапс 1 степени приходится
свыше 90% случаев и практически всегда он гемодинамически незначим.
Клиническая (гемодинамическая) значимость ПМК определяется тяжестью
митральной регургитации (недостаточности). Чем выше степень пролапса, тем
большее количество крови регургитирует (возвращается) в левое предсердие,
что соответственно повышает клиническую значимость этой аномалии. Наблюдения
требуют пациенты: 1) с пролапсом 2 или 3 степени; 2) если створки
митрального клапана миксоматозно изменены; 3) если ПМК сочетается с
множественными дополнительными хордами в левом желудочке. Обозначенная
категория лиц находится в группе риска в плане формирования в будущем
развернутой болезни сердца (порок сердца или аритмический синдром). Лица с
ПМК 1 степени и без дополнительных аномалий в диспансеризации не нуждаются -
они здоровы.
УЗИ сердца
позволяет визуализировать ПМК, оценить его степень и гемодинамическую
значимость.
Синдром (феномен)
WPW -
микропорок сердца, сущность которого состоит
в наличии дополнительного проводящего пути между предсердиями и желудочками.
В норме электрическая коммуникация между ними осуществляется через так
называемый атриовентрикулярный узел. В результате нарушения внутриутробного
развития в сердце (помимо названного узла) функционируют дополнительные
мышечно-проводящие пучки (пучки Кента), связывающие предсердия и желудочки.
Как правило, пучок один, реже - два и больше. Такая ненормальность приводит
к тому, что электрическое возбуждение от предсердий к желудочкам идет по 2
путям: нормальному (АВ-узел) и аномальному (пучок Кента). Клиническая значимость данного микропорока сердца определяется возможным
возникновениям приступов немотивированного сердцебиения (атриовентрикулярные
реципрокные тахикардии - циркуляция электрического импульса с участием пучка
Кента). Синдром WPW выявляется на обычной
ЭКГ и при отсутствии приступов сердцебиения называется феноменом
WPW. Человек может прожить десятилетия с такой "плохой
кардиограммой", оставаясь субъективно абсолютно здоровым. Первый в
жизни пароксизм тахикардии автоматически переводит феномен
WPW в синдром - то есть в болезнь. Феномен
WPW начинает выявляется на ЭКГ чаще всего между 10
и 30 годами. Время его перехода в синдром (появление пароксизмов
сердцебиения) вариабельно и непредсказуемо. У кого-то "трансформация"
занимает несколько месяцев, у кого-то десятилетия. Чем раньше наступает
электрокардиографическая манифестация феномена
WPW, тем выше вероятность появления в течении
жизни приступов аритмии. Другими словами, если феномен
WPW появляется на ЭКГ у лиц старших возрастных групп (за 40 лет), то
вероятность возникновения аритмий у них весьма мала, поскольку они просто
могут не дожить до стадии синдрома, умирая от каких-либо естественных
причин. Лечебная тактика в отношении синдрома WPW
в России и зарубежом отличается. В экономически развитых странах при его
выявлении у лиц молодого и среднего возраста все больше закрепляется
активная лечебная тактика: рекомендована радиочастотная абляция пучка Кента
на бессимптомной стадии заболевания (на этапе феномена). Такой подход
основан на том, что синдром
WPW, как было установлено, на какую-то долю процента повышает риск
внезапной сердечной смерти. Поэтому абляция пучка избавляет пациента от
будущих аритмий и нивелирует другие сердечные риски. В России операция
абляции при синдроме WPW выполняется только при
появлении приступов реципрокной аритмии (хотя бы одного) - то есть на стадии
синдрома. Мои рекомендации пациентам с феноменом WPW:
1) жить обычной жизнью - первый приступ сердцебиения, если и возникнет, то
застанет вас врасплох, поэтому не стоит о нем думать. Сам приступ
практически не несет угрозы для жизни. При его появлении 2) следует
немедленно перейти в состояние физического покоя, вызвать скорую медицинскую
помощь для снятия приступа и документации аритмии посредством ЭКГ, 3) после
купирования первого пароксизма сердцебиения необходимо планово обратиться в
поликлинику к кардиологу.
Клиническая значимость данного микропорока сердца определяется возможным
возникновениям приступов немотивированного сердцебиения (атриовентрикулярные
реципрокные тахикардии - циркуляция электрического импульса с участием пучка
Кента). Синдром WPW выявляется на обычной
ЭКГ и при отсутствии приступов сердцебиения называется феноменом
WPW. Человек может прожить десятилетия с такой "плохой
кардиограммой", оставаясь субъективно абсолютно здоровым. Первый в
жизни пароксизм тахикардии автоматически переводит феномен
WPW в синдром - то есть в болезнь. Феномен
WPW начинает выявляется на ЭКГ чаще всего между 10
и 30 годами. Время его перехода в синдром (появление пароксизмов
сердцебиения) вариабельно и непредсказуемо. У кого-то "трансформация"
занимает несколько месяцев, у кого-то десятилетия. Чем раньше наступает
электрокардиографическая манифестация феномена
WPW, тем выше вероятность появления в течении
жизни приступов аритмии. Другими словами, если феномен
WPW появляется на ЭКГ у лиц старших возрастных групп (за 40 лет), то
вероятность возникновения аритмий у них весьма мала, поскольку они просто
могут не дожить до стадии синдрома, умирая от каких-либо естественных
причин. Лечебная тактика в отношении синдрома WPW
в России и зарубежом отличается. В экономически развитых странах при его
выявлении у лиц молодого и среднего возраста все больше закрепляется
активная лечебная тактика: рекомендована радиочастотная абляция пучка Кента
на бессимптомной стадии заболевания (на этапе феномена). Такой подход
основан на том, что синдром
WPW, как было установлено, на какую-то долю процента повышает риск
внезапной сердечной смерти. Поэтому абляция пучка избавляет пациента от
будущих аритмий и нивелирует другие сердечные риски. В России операция
абляции при синдроме WPW выполняется только при
появлении приступов реципрокной аритмии (хотя бы одного) - то есть на стадии
синдрома. Мои рекомендации пациентам с феноменом WPW:
1) жить обычной жизнью - первый приступ сердцебиения, если и возникнет, то
застанет вас врасплох, поэтому не стоит о нем думать. Сам приступ
практически не несет угрозы для жизни. При его появлении 2) следует
немедленно перейти в состояние физического покоя, вызвать скорую медицинскую
помощь для снятия приступа и документации аритмии посредством ЭКГ, 3) после
купирования первого пароксизма сердцебиения необходимо планово обратиться в
поликлинику к кардиологу.
Легочная гипертензия - синдром, в основе которого лежит повышение давления крови в легочной артерии; в результате правые камеры сердца вынуждены работать с повышенной нагрузкой, чтобы "протолкнуть" кровь через "участок" высокого давления. Напомню, что кровь из периферических вен стекается в правые камеры сердца, оттуда через легочную артерию поступает в систему легочных капилляров, где происходит обогащение ее (крови) кислородом; из легких кровь по системе легочных вен доставляется в левые отделы сердца. При легочной гипертензии формируется препятствие кровотоку на уровне легочной артерии или (и) ее ветвей. Это всегда вторичная патология. Заболевания, могущие осложниться легочной гипертензией: 1) Клапанные пороки и заболевания левых камер сердца - самая распространенная причина легочной гипертензии. При поражении левого желудочка (например, после перенесенного инфаркта миокарда) он становится не в состоянии перекачать весь объем крови, который притекает к нему из легких. Кровь начинает застаиваться в системе легочной артерии, что приводит к повышению в ней давления. Теоретически любое серьезное органическое заболевание левого желудочка, пороки митрального или аортального клапанов могут со временем осложниться легочной гипертензией; 2) ТЭЛА - очень частая причина легочной гипертензии. Попадающие в систему легочной артерии тромботические массы перекрывают часть её просвета, что приводит к значительному повышению давления в ней и снижению кровотока через легкие; 3) Заболевания бронхоальвиолярной системы, приводящие к развитию легочной гипертензии. К этой группе относятся патологии, поражающие легочную ткань или (и) мелкие бронхи: бронхиальная астма, хронический обструктивный бронхит и др. Естественным следствием длительного патологического процесса в легких и бронхах является тканевой склероз, в результате которого происходит замещение мелких легочных артерий на соединительную ткань, что, в свою очередь, уменьшает общее "поперечное сечение" русла легочной артерии и постепенно приводит к повышению давления в ней; 4) Врожденные пороки сердца. Большинство из них сопровождаются перегрузкой правых камер сердца "объемом", приводящей к легочной гипертензии; 5) Системные заболевания (амилоидоз, саркоидоз и др.), которые через много лет могут давать осложнения на легкие в виде диффузного склероза ее паренхимы и замещению легочных артериол соединительной тканью. В этом случае патофизиология легочной гипертензии такая же, как при первичных заболеваниях бронхоальвеолярной системы.
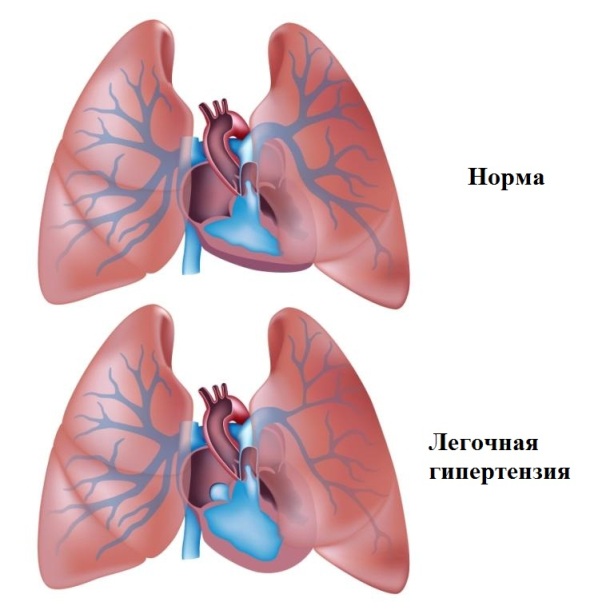
Основным клиническим проявлением легочной гипертензии является одышка при незначительной физической нагрузке. Наличие легочной гипертензии указывает на далеко зашедшую стадию основного заболевания, отражая запущенность процесса и неблагоприятный прогноз. Эффективного лечения стойкой легочной гипертензии не существует - необходимо своевременно лечить основное заболевание.
Синдром укороченного интервала P-Q - представляет собой феномен, распознаваемый специалистом исключительно на ЭКГ. Данный синдром, при его выявлении, часто служит поводом для направления к кардиологу. О сути синдрома... Электрическое сообщение миокарда предсердий и миокарда желудочков осуществляется через АВ-узел. Электрический импульс проходит через него с небольшой задержкой (доли секунды), которая (задержка) на ЭКГ отражается в виде так называемого интервала P-Q.
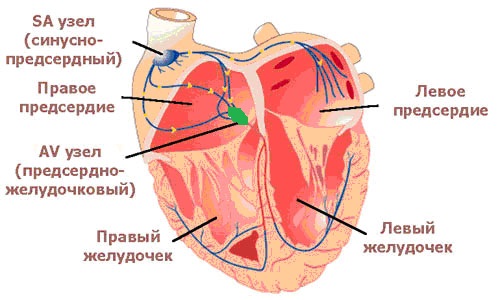
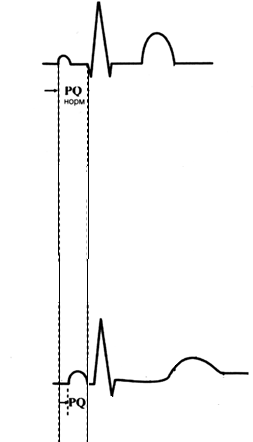 Такая задержка необходима для последовательного сокращения камер сердца
(сначала предсердий, затем желудочков), что делает внутрисердечную
гемодинамику более выгодной. Он (интервал) имеет верхнюю и нижнюю границу
нормы. Его величина меньше нормальной в кардиологии обозначается синдромом
укороченного P-Q. Опасно ли это? Раньше (еще лет
10-15 назад) считалось, что данный ЭКГ-паттерн ассоциируется с
возникновением приступов сердцебиения (пароксизмальные тахикардии);
отношение к нему было такое же как к
синдрому
WPW. Однако
впоследствии было доказано, что данный синдром не провоцирует никаких
аритмий и по сути является просто ЭКГ-аномалией. Короткий интервал
P-Q является нормой для детей малого возраста, поэтому если он
(интервал) таковым остается у взрослого, то это считается признаком
"инфантильности" АВ-узла. Единственное клиническое значение данного феномена
заключается в том, что если у взрослого в будущем когда-нибудь разовьется
фибрилляция предсердий
(мерцательная аритмия), то высока вероятность того, что она (аритмия) будет
протекать с высокой частотой сокращения желудочков из-за неспособности
АВ-узла к "задержке" импульсов. Лица с синдромом укороченного
P-Q не нуждаются в кардиологической
диспансеризации.
Такая задержка необходима для последовательного сокращения камер сердца
(сначала предсердий, затем желудочков), что делает внутрисердечную
гемодинамику более выгодной. Он (интервал) имеет верхнюю и нижнюю границу
нормы. Его величина меньше нормальной в кардиологии обозначается синдромом
укороченного P-Q. Опасно ли это? Раньше (еще лет
10-15 назад) считалось, что данный ЭКГ-паттерн ассоциируется с
возникновением приступов сердцебиения (пароксизмальные тахикардии);
отношение к нему было такое же как к
синдрому
WPW. Однако
впоследствии было доказано, что данный синдром не провоцирует никаких
аритмий и по сути является просто ЭКГ-аномалией. Короткий интервал
P-Q является нормой для детей малого возраста, поэтому если он
(интервал) таковым остается у взрослого, то это считается признаком
"инфантильности" АВ-узла. Единственное клиническое значение данного феномена
заключается в том, что если у взрослого в будущем когда-нибудь разовьется
фибрилляция предсердий
(мерцательная аритмия), то высока вероятность того, что она (аритмия) будет
протекать с высокой частотой сокращения желудочков из-за неспособности
АВ-узла к "задержке" импульсов. Лица с синдромом укороченного
P-Q не нуждаются в кардиологической
диспансеризации.
Синусовая аритмия.
Регулярность сердечного ритма относительна. В
норме присутствует небольшая вариабельность (речь идет о долях секунды),
которая субъективно не ощущается, однако с легкостью выявляется на ЭКГ. Это
и есть синусовая аритмия. Существует 2 ее клинические разновидности: 1)
физиологическая - присутствует у любого здорового человека. Крайним
вариантом такой аритмии является дыхательная (циклическая) синусовая
аритмия: на вдохе сердечный ритм учащается, на выдохе - урежается. При
дыхательной аритмии колебания сердечного ритма, кроме того что они связаны с
актом дыхания, более выражены. Циклическая синусовая аритмия характерна для
молодых лиц с кардионеврозом и тренированных спортсменов. 2) нециклическая
синусовая аритмия часто выявляется у пожилых людей с системным
атеросклерозом, когда нарушается функционирование мозговых центров регуляции
сердечного ритма. Она не связана с дыханием и, вероятно, является одним из
проявлений старения организма.
Синусовая аритмия у юноши 17 лет в период ночного сна.
Синусовая аритмия, какого бы происхождения она не была, не требует лечения. Напротив, следует опасаться чрезмерно регулярного сердечного ритма (ригидный синусовый ритм), когда естественные колебания практически не наблюдаются. Всегда стоит помнить фундаментальный закон диалектического единства: противоположности должны сочетаясь, динамически уравновешивать, дополнять друг друга. Другими словами, синусовый ритм не должен быть слишком регулярным (преобладание одной противоположности), поскольку это ассоциируется с желудочковыми нарушениями ритма и повышенным риском сердечно-сосудистой смерти. Однако спешу вас успокоить: ригидный синусовый ритм характерен для тяжелых хроников-сердечников. Подведем итог: даже если врач встречается с выраженными проявлениями синусовой аритмии, внимание на ней акцентироваться не будет.
Открытое овальное окно - естественное анатомическое сообщение между правым и левым предсердием, в норме присутствующее только у плода.
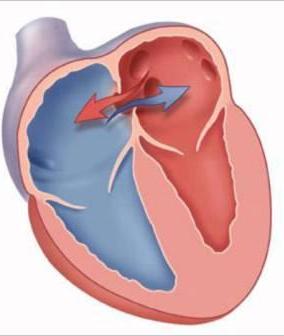 После
рождения это отверстие в течение не более года зарастает. В случае
если оно остается открытым, то речь идет о пороке сердца. Сроки клинической
манифестации порока (симптомы сердечной недостаточности) зависят от размера
дефекта (окна). Если дефект малый, то симптомы могут появиться только в
зрелом возрасте (за 40 лет); в случае значительного дефекта - симптомы
возникают в детском возрасте. Диагностируется порок с помощью
УЗИ сердца. Иногда, если дефект очень мал
или визуализация сердца плохая, обычное УЗИ сердца оказывается
неинформативным - тогда применяют
чрезпищеводное УЗИ сердца. Лечение порока
только оперативное. В настоящее время стараются использовать малоинвазивную
методику - катетерная имплантация "заплатки" в место открытого овального
окна.
После
рождения это отверстие в течение не более года зарастает. В случае
если оно остается открытым, то речь идет о пороке сердца. Сроки клинической
манифестации порока (симптомы сердечной недостаточности) зависят от размера
дефекта (окна). Если дефект малый, то симптомы могут появиться только в
зрелом возрасте (за 40 лет); в случае значительного дефекта - симптомы
возникают в детском возрасте. Диагностируется порок с помощью
УЗИ сердца. Иногда, если дефект очень мал
или визуализация сердца плохая, обычное УЗИ сердца оказывается
неинформативным - тогда применяют
чрезпищеводное УЗИ сердца. Лечение порока
только оперативное. В настоящее время стараются использовать малоинвазивную
методику - катетерная имплантация "заплатки" в место открытого овального
окна.
"Диффузные изменения в миокарде левого желудочка". Эта идиома часто встречается в описании электрокардиограммы, с которой пациент приходит к кардиологу на прием. Таким словосочетанием врачей функциональной диагностики учат описывать любые трудноинтерпретируемые и неспецифические изменения на ЭКГ, отражающие электрическую активность левого желудочка. Мое отношение к нему - крайне негативное. Как я уже упоминал на страницах сайта, обычная ЭКГ отличается в целом низкой чувствительностью и низкой специфичностью в отношении многих заболеваний сердца. Думаю, что для пациента это звучит удивительно, но ЭКГ может стереотипно меняться при множестве сердечных и несердечных (!) заболеваниях. Так вот такие изменения, которые не укладываются в какой-то определенный ЭКГ-диагноз, как правило, интерпретируют, как "диффузные изменения в миокарде левого желудочка". В основном это касается зубца "Т" на ЭКГ. Есть даже такое выражение: "болезней много, а зубец Т один". А по-другому можно сказать: при множестве заболеваний зубец Т изменяется одинаково. Я отношусь отрицательно к обсуждаемой словосочетанию, потому что заметил: оно тревожит и беспокоит пациентов, которые, прочитав такое ЭКГ-заключения, становятся мнительными; хотя изменения на ЭКГ, по-сути, могут совершенно не отражать "плохого состояния сердца". Иногда одно неверно сказанное или некорректно написанное слово может спровоцировать или усугубить невроз. Выражение "диффузные изменения..." я обычно заменяю на "неспецифические изменения в миокарде левого желудочка", либо, описываю ЭКГ буквально, например: "отрицательные зубцы Т там то, там-то...."
Радиочастотная катетерная абляция (РЧА). Современный хирургический способ лечения сердечных аритмий, не поддающихся лекарственной коррекции. При этом методе все инструментальные манипуляции осуществляются через прокол одной из крупных вен (чаще подключичной). Через вену лечебный катетер доставляют до аритмического очага, на который воздействуют высокочастотной энергией - это приводит к деструкции "фокуса аритмии".
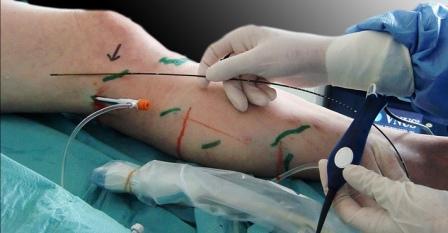
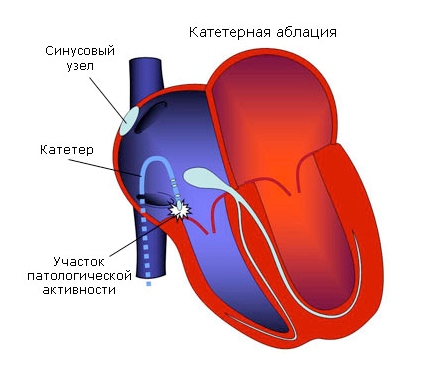 Важнейшим преимуществом РЧА перед традиционными полостными
кардиохирургическими операциями, является ее малоинвазивность - манипуляция
осуществляется без вскрытия грудной клетки, без общего наркоза, без
последующего длительного заживления операционного шва и физической
реабилитации. Изначально РЧА использовали для радикального лечения пациентов
с
синдромом
WPW.
Действительно, деструкция дополнительного пучка с помощью локального
воздействия высокочастотной электрической энергии приводило к блестящему
клиническому результату: полному выздоровлению больного. В дальнейшем спектр
показаний к выполнению РЧА существенно расширился. Сейчас она используется
для лечения фибрилляции и трепетания предсердий, идиопатической желудочковой
и предсердной экстрасистолии, АВ-реципрокной тахикардии и др. Те пациенты,
которые раньше всю жизнь мучались от тягостных приступов сердцебиения и
перебоев в работе сердца с внедрением методики РЧА получили шанс на полное
выздоровление. Максимальный лечебный эффект (отсутствие рецидива в
отдаленном послеоперационном периоде) при РЧА прослеживается у пациентов без
признаков органического поражения миокарда.
Важнейшим преимуществом РЧА перед традиционными полостными
кардиохирургическими операциями, является ее малоинвазивность - манипуляция
осуществляется без вскрытия грудной клетки, без общего наркоза, без
последующего длительного заживления операционного шва и физической
реабилитации. Изначально РЧА использовали для радикального лечения пациентов
с
синдромом
WPW.
Действительно, деструкция дополнительного пучка с помощью локального
воздействия высокочастотной электрической энергии приводило к блестящему
клиническому результату: полному выздоровлению больного. В дальнейшем спектр
показаний к выполнению РЧА существенно расширился. Сейчас она используется
для лечения фибрилляции и трепетания предсердий, идиопатической желудочковой
и предсердной экстрасистолии, АВ-реципрокной тахикардии и др. Те пациенты,
которые раньше всю жизнь мучались от тягостных приступов сердцебиения и
перебоев в работе сердца с внедрением методики РЧА получили шанс на полное
выздоровление. Максимальный лечебный эффект (отсутствие рецидива в
отдаленном послеоперационном периоде) при РЧА прослеживается у пациентов без
признаков органического поражения миокарда.
Синусовая тахикардия - учащение сердечного ритма свыше 90 ударов в минуту. В состоянии покоя сердце здорового человека сокращается с частотой 50-80 ударов в минуту. Причины синусовой тахикардии: 1. Естественная реакция организма (сердца) на физическую или психоэмоциональную (гнев, крик, страх) нагрузку. Все бегали стометровку? Все сдавали экзамен в школе? Это ситуации, когда организму требуется больше энергии; в таком случае учащение сердечного ритма обеспечивает доставку к органам и тканям нужного количества кислорода. 2. Синусовая тахикардия нередко наблюдается у лиц с кардионеврозом, для которых характерно постоянное, фоновое волнение - пациенты могут жаловаться на сердцебиение. 3. Немотивированная синусовая тахикардия иногда наблюдается при злоупотреблении алкоголем, дисгормональной кардиомиопатии, беременности, гипертиреозе и некоторых других клинических ситуациях. 4. Синусовая тахикардия возникает у больных с тяжелым органическим поражением миокарда, осложнившейся сердечной недостаточностью; например: после перенесенного инфаркта миокарда, длительная диастолическая дисфункция левого желудочка. В таких ситуациях учащение ритма является компенсаторным механизмом, возникающим в ответ на "слабость сердечной мышцы" - пораженное сердце вынужденно сокращаться чаще, чтобы обеспечить потребности организма в кислороде. 5. Тяжелые заболевания бронхолегочной системы, когда легкие не могут обеспечить насыщение крови кислородом в нужном количестве - дыхательная недостаточность. Тогда сердце начинает сокращаться чаще, чтобы компенсировать гипооксигенацию крови.
Блокада ножки пучка Гиса. Нередко пациенты вычитывают на выданных им ЭКГ заключение "о блокаде какой-то там ножки". Осознание наличия "блокады сердца" многих вводит в состояние когнитивного диссонанса. Частью проводящей системы сердца, обеспечивающей проведение электрического возбуждения от предсердий к желудочкам, являются так называемые ножки пучка Гиса.
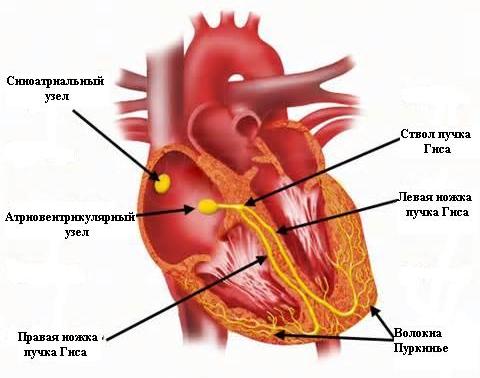 Их
две: правая (идет к правому желудочку) и левая (идет к левому желудочку).
Левая ножка имеет переднюю и заднюю ветвь. Проведение по каждой из ножек
может быть замедленно или прервано полностью. В первом случае говорят о
неполной блокаде, во втором - о полной. Блокада левой ножки абсолютно не
характерна для здорового сердца. Остальные варианты блокад (правой
ножки, передней или задней ветви левой ножки) могут быть как проявлением
болезни, так и встречаться у здоровых людей, в виде невинной врожденной
аномалии проводящей системы сердца, выявляемой на ЭКГ. Впрочем, последняя
категория лиц, на мой взгляд, нуждаются в ненавязчивом наблюдении кардиолога
для отслеживания динамики ЭКГ-блокады и самочувствия - изредка такие
нарушения проводимости прогрессируют.
Их
две: правая (идет к правому желудочку) и левая (идет к левому желудочку).
Левая ножка имеет переднюю и заднюю ветвь. Проведение по каждой из ножек
может быть замедленно или прервано полностью. В первом случае говорят о
неполной блокаде, во втором - о полной. Блокада левой ножки абсолютно не
характерна для здорового сердца. Остальные варианты блокад (правой
ножки, передней или задней ветви левой ножки) могут быть как проявлением
болезни, так и встречаться у здоровых людей, в виде невинной врожденной
аномалии проводящей системы сердца, выявляемой на ЭКГ. Впрочем, последняя
категория лиц, на мой взгляд, нуждаются в ненавязчивом наблюдении кардиолога
для отслеживания динамики ЭКГ-блокады и самочувствия - изредка такие
нарушения проводимости прогрессируют.
Синдром ранней реполяризации желудочков (РРЖ). Едва ли не у четверти всех людей на ЭКГ обнаруживают, так называемый, синдром ранней реполяризации желудочков. Пациенты часто приходят к кардиологу с вопросом, что же он означает? Данный ЭКГ-феномен отражает локальную неоднородность сердечной реполяризации и носит врожденный характер. В подавляющем большинстве случаев он абсолютно безопасен и относиться к нему следует, как, например, к пролапсу митрального клапана 1 ст., синдрому укороченного интервала P-Q, дополнительной хорде левого желудочка - то есть как к невинной сердечной аномалии. Однако, на какую-то долю процента (~0,1%) этот синдром, повышает риск внезапной сердечной смерти через запуск идипатической фибрилляции желудочков - со стороны это выглядит, как внезапная смерть абсолютно здорового молодого человека. О таких шокирующих эпизодах мы регулярно слышим из СМИ. В медицинских журналах также описываются инциденты злокачественного течения синдрома РРЖ с летальным исходом. Однако, априорная вероятность его неблагоприятного течения составляет менее 1%. Одним из возможных маркеров потенциальной опасности синдрома является изменение степени преждевременности реполяризации (то есть на разных ЭКГ проявления синдрома имеют разную степень выраженности), особенно в сочетании с синкопальным анамнезом.
"Витамины для сердца". Неоднократно в своей практической деятельности приходилось сталкиваться с настойчивостью пациента, убеждающего меня назначить ему какие-нибудь "витамины для сердца". Особый напор ощущается от лиц с кардионеврозом. Не знаю откуда все это люди вычитывают, но никаких "витаминов укрепляющих сердечную мышцу" нет. Судя по всему, в заблуждение простого обывателя вводят СМИ (в том числе интернет), рекламирующие подобные препараты в контексте их "кардиометаболического эффекта". Зачастую, такие пациенты уже были ранее у кардиологов; они им прописывали Магний В6, Предуктал, Милдронат, Магнерот, Кудесан и прочее. Видимо, подобные препараты и расцениваются кем-то в качестве "витаминов для сердца". Обозначенные лекарства имеют свою нишу применения в кардиологии, и вкратце она выглядит следующим образом: антиаритмический эффект (речь идет о магний-чувствительной экстрасистолии); антиишемический эффект (препараты типа Предуктала показаны больным с тяжелой стенокардией); эффект плацебо - пациент хочет лечиться - пусть лечиться(!), но указанные лекарства будут действовать на уровне самовнушения.
Варфарин - антикоагулянт; препятствует образованию тромбов, способствует растворению уже существующих. В отличие от аспирина основная точка приложения варфарина: 1) профилактика венозных тромбозов, 2) профилактика тромбообразования в полостях сердца. В кардиологии варфарин используют в 3-х клинических ситуациях: ТЭЛА, мерцательная аритмия (фибрилляция предсердий) и наличие протезированного сердечного клапана. При ТЭЛА венозные тромбы, образующиеся в венах малого таза и нижних конечностей, отрываясь, с током крови заносятся в ветви легочной артерии. Назначение антикоагулянтов в такой ситуации является одним из обязательных компонентов лечения, направленного на предупреждение пролонгации тромбооразования в венах и лизиса тромботических масс, занесенных в легочную артерию. При мерцательной аритмии отсутствует эффективное сокращение предсердий, что создает условия для стаза, завихрения крови в так называемом ушке левого предсердий. Ушко левого предсердия - трабекулярная, замкнутая полость в которой легко формируются тромботические массы. От внутрипредсердного тромба, хронологически непредсказуемо, могут отрываться "кусочки" и залетать (эмболия) в разные органы; самая драматичная ситуация - тромбоэмболия мозговой артерии - означает инсульт. Однако, далеко не у всех, кто страдает мерцательной аритмией в левом предсердии образуются тромбы. В группе риска находятся: 1) лица с постоянной формой фибрилляции предсердий или с часто рецидивирующими (чаще раз в месяц) приступами аритмии (особенно субъекты старше 60 лет; чем старше, тем выше риск тромбообразования); 2) пациенты с расширенным левым предсердием (определяется при УЗИ сердца); 3) больные с дополнительными факторами риска повышенного тромбообразования: сахарный диабет, ожирение, перенесенный инфаркт миокарда и др. Протезированный сердечный клапан является чрезвычайно тромбогенным; потенциальное осложнение такое же как при мерцательной аритмии: тромбоэмболии. Пациенты с протезированным клапаном принимают варфарин в высоких дозировках. Лечение Варфарин проводится только под контролем МНО (международное нормализованное отношение). МНО - это относительный показатель, отражающий силу антикоагулянтного эффекта варфарина. Кровь на МНО сдается в любой маломальской лаборатории. Терапевтическим считается МНО от 2 до 3,5 - только при таком диапазоне МНО новые тромбы не образуются, а старые растворяются. Если МНО меньше 2-х, считайте, что варфарин принимается вхолостую. При МНО свыше 3,5-х возникает угроза кровотечения - в таком случае риск от его использования превышает пользу. Необходимость регулярно сдавать анализ крови на МНО, вместе с лабильностью этого параметра и является краеугольным камнем в лечении варфарином. Порой, сложно достичь целевого значения МНО, а при его достижении через некоторое время оно, вдруг, выходит за допустимые границы. При "оттитрованном" МНО анализ крови сдается всего раз в 4-6 месяцев. В последние годы были созданы новые антикоагулянты, не требующие лабораторного контроля (не нужно ходить в поликлинику сдавать анализ крови) - в этом их колоссальное преимущество перед варфарином. В России широко используются Прадакса и Ксарелто. Главный недостаток этих препаратов - цена: месячный курс лечения будет обходиться примерно в 3000-4000 рублей, что в 10 раз превышает стоимость лечения варфарином. Подчеркну, что если на фоне терапии варфарином достигнуто целевое МНО и оно таковым остается постоянно, то эффективность антикоагулянтного лечения абсолютна сопоставима с таковым при применении новых антикоагулянтов. Таким образом, для "бюджетных" пациентов варфарин по-прежнему остается препаратом выбора. Жизнь с Вафарином.
Дисгормональная (климактерическая) кардиомиопатия. Климакс - естественное увядание репродуктивной функции человека. Большинство людей переживают этот период благополучно или с умеренно выраженной неприятной симптоматикой. Патологический климакс сопровождается целым спектром тягостных ощущений, которые заметно ухудшают качество жизни и вынуждают обратиться к врачу. Одним из проявлений патологического течения климакса может оказаться дисгормональная кардиомиопатия. Половые гормоны, являясь естественными кардиопротекторами, играют важную роль в метаболизме сердечной мышцы, поэтому их нехватка в период угасания репродуктивной функции лежит в основе развития кардиомиопатии. Это заболевание представляет собой сочетание неспецифических симптомов климакса (вегетативные кризы и изменение в нервно-психической сфере) и кардиальной симптоматики. Вегетативные проявления: приливы, повышенная потливость, ощущение онемения в разных частях тела, головокружения. Нервно-психические симптомы: повышенная раздражительность, слезливость, бессонница, неустойчивое настроение, неудовлетворенность вдохом, немотивированная слабость. Кардиальная симптоматика складывается из симптомов, как при кардионеврозе (кардиалгия, ощущение сердцебиения, экстрасистолия) и изменений на ЭКГ ("плохая ЭКГ"). Хронология появления субъективной симптоматики при женском и мужском климаксе разная. У женщин симптомы дисгормональной кардиомиопатии могут начаться с 35-37 лет (то есть задолго до нарушений менструального цикла и собственно климакса) или, наоборот, появиться на 6-м десятке жизни (то есть через несколько лет после наступления климакса). Таким образом, подчеркиваю, появление симптомов патологического женского климакса не всегда коррелируют с "типичным климактерическим возрастом" - 40-50 лет. Возраст наступления мужского климакса менее предсказуем, но в отличие от женского его симптоматика более или менее четко увязывается со снижением либидо и прогрессирующим нарушением копулятивной способности (эректильная дисфункция вплоть до импотенции). Другое дело, что мужчины, страдающие дисгормональной кардиомиопатией, зачастую, скрывают от кардиолога свои интимные проблемы, не понимая их связь с сердечными симптомами, что затрудняет диагностику. Лечение патологического климакса напоминает таковое при кардионеврозе. Во-первых, необходимо доходчиво объяснить суть проблемы, ее безопасность и полную обратимость заболевания (дисгормональная кардиомиопатия самостоятельно проходит через 1-5 лет). Во-вторых, при необходимости назначают седативные средства (начиная с травяных настоек, заканчивя рецептурными препаратами). В-третьих, при аритмических симптомах (сердцебиение, перебои) возможно назначение кардиотропных лекарств, купирующих эти ощущения. В-четвертых, при неэффективности указанных выше мероприятий больному показана заместительная гормональная терапия под контролем уролога или гинеколога. Однако, потребность в гормональной терапии патологического климакса в последние годы не возникает, так как практически всегда удается справиться "негормональными средствами". В заключение подчеркну еще раз: дисгормональная кардиомиопатия - функциональное, полностью обратимое заболевание сердца, исходом которого является полное выздоровление.
Чрезпищеводное ЭФИ сердца (электрофизиологическое исследование). Метод изучения некоторых электрофизиологических параметров сердца, возможный благодаря анатомическому прилеганию средней трети пищевода к сердцу, точнее к левому предсердию. Методология исследования: через ротовую полость в пищевод вводят специальный электрод до места соприкосновения его с сердцем; затем по специальному протоколу начинают подавать электрические импульсы, проходящие от пищевода к сердцу. Характер ответа сердца (определяемый по ЭКГ) на навязанную ему извне импульсацию и является объектом изучения. ЧПЭФИ показано 1) при подозрении на синдром слабости синусового узла (блокада сердца), 2) при подозрении на нарушение атриовентрикулярной проводимости (блокада сердца), 3) при подозрении на наличие реципрокных наджелудочковых аритмий с участием АВ-узла, 4) при подозрении на синдром WPW. Врач может вам предложить провести ЧПЭФИ, если вас беспокоят обмороки (полуобморочные состояния) и приступы сердцебиения неясной этиологии; как правило, этому специфическому исследованию предшествует холтеровское мониторирование ЭКГ, которое не дало однозначного ответа на поставленные вопросы. Кроме того, чрезпищеводный электрод иногда используют в лечебных целях: посредством чрезпищеводной стимуляции сердца купируются некоторые наджелудочковые тахиаритмии.
Чрезпищеводное УЗИ сердца. Известно, что при обычном УЗИ сердца, именуемым трансторакальным, датчик прикладывается к грудной клетке. При этом от структур сердца ультразвуковой датчик "отделен" кожей, межреберными мышцами, ребрами, легкими. Таким образом, чтобы "добраться до места назначения", ультразвуку необходимо пройти сквозь несколько анатомических препятствий разной плотности, что снижает качество ультразвуковой картинки.
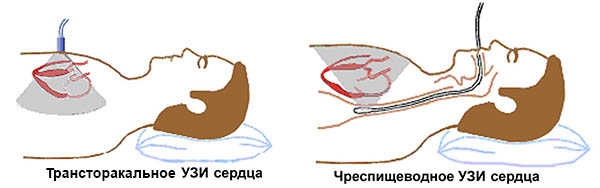 Существует
альтернативная методология визуализации сердца посредством ультразвука,
возможная благодаря анатомическому прилеганию средней трети пищевода к
сердцу. Через ротовую полость специальный чрезпищеводный датчик вводят в
пищевод до соприкосновения его с сердцем; от этого места ультразвук с
минимальными искажениями "добирается" до сердечных структур - визуализация
сердца получается практически идеальной. Проведение чрезпищеводного УЗИ
сердца показано в тех случаях, когда обычное УЗИ не дает ответы на
поставленные вопросы. А это: 1) диагностика тромбов в полостях сердца
(главным образом, в ушке левого предсердия при мерцательной аритмии), 2)
оценка функции протезированного клапана (например, при подозрении на его
эндокардит или тромбообразование на нем), 3) диагностика патологии аорты
(например, расслаивающая аневризма), 4) подозрение на инфекционный
эндокардит, неподтвержденное обычным УЗИ, 5) точная диагностика
некоторых врожденных пороков сердца (дефект межпредсердной перегородки,
двухстворчатый аортальный клапан), длительно не вызывающих нарушение
гемодинамики.
Существует
альтернативная методология визуализации сердца посредством ультразвука,
возможная благодаря анатомическому прилеганию средней трети пищевода к
сердцу. Через ротовую полость специальный чрезпищеводный датчик вводят в
пищевод до соприкосновения его с сердцем; от этого места ультразвук с
минимальными искажениями "добирается" до сердечных структур - визуализация
сердца получается практически идеальной. Проведение чрезпищеводного УЗИ
сердца показано в тех случаях, когда обычное УЗИ не дает ответы на
поставленные вопросы. А это: 1) диагностика тромбов в полостях сердца
(главным образом, в ушке левого предсердия при мерцательной аритмии), 2)
оценка функции протезированного клапана (например, при подозрении на его
эндокардит или тромбообразование на нем), 3) диагностика патологии аорты
(например, расслаивающая аневризма), 4) подозрение на инфекционный
эндокардит, неподтвержденное обычным УЗИ, 5) точная диагностика
некоторых врожденных пороков сердца (дефект межпредсердной перегородки,
двухстворчатый аортальный клапан), длительно не вызывающих нарушение
гемодинамики.
Аномально расположенная хорда (АРХ). От свободных концов створок митрального клапана идут так называемые хорды, которые крепятся другим концом к стенкам левого желудочка. Хорда представляет собой тонкий (2-3 мм) соединительнотканный тяж, опосредованно участвующий в открытии и закрытии клапана.
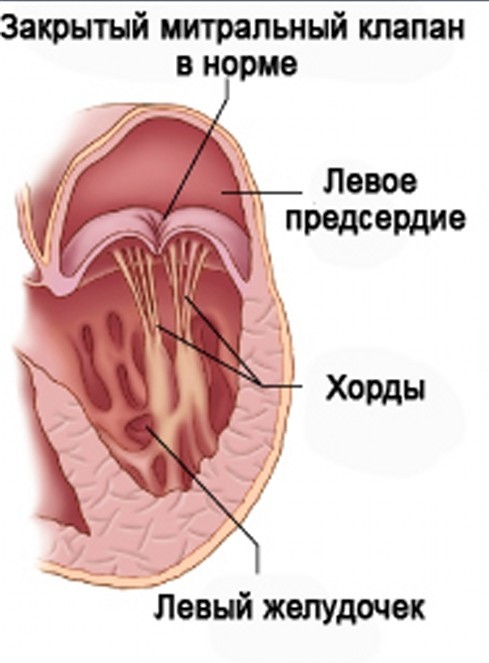
Когда левый желудочек сокращается (систола) - натяжение хорд ослабевает -
клапан плотно закрывается; когда левый желудочек расслабляется (диастола) -
хорды "тянуться" за "расправленным" желудочком - клапан открывается. Отрыв
хорды (например, при инфаркте миокарда) приводит к тому, что в систолу
желудочка створка митрального клапана начинает пролабировать (провисать) в
полость левого предсердия; в такой ситуации клапан закрывается негерметично
и часть крови возвращается (регургитирует) в левое предсердие.
АРХ - это хорда, которая "натянута" между стенками левого
желудочка. Такая хорда не выполняет никакой функции, из-за своего
аномального расположения; она просто присутствует в сердце, как
дополнительный тяж. Примерно 80% (!) людей имеют хотя бы одну АРХ. По
современным представлениям клиническое значение АРХ приближается к нулю - то
есть ее наличие ничем не грозит. Исключением являются только случаи
полихордальности (когда в левом желудочке обнаруживают больше, чем одну АРХ)
или когда АРХ представляет собой не соединительнотканный, а мышечный тяж
("толстая" хорда). Предполагают, что у таких субъектов на какую-то долю
процента увеличивается риск
внезапной сердечной смерти в молодом
возрасте (до 30 лет). Если для примера взять 10000 лиц без АРХ и 10000 с АРХ,
то во второй группе 1 человек хронологически непредсказуемо внезапно умрет в
молодости. Возможно, лица с полихордальностью или с наличием "мышечной"
хорды имеют еще более высокий риск внезапной сердечной смерти. АРХ
диагностируют посредством УЗИ
сердца. Однако, даже при наличии АРХ обнаружить ее удается не
всегда - многое зависит от опыта и педантизма врача.
Систолическое (верхнее) артериальное давление (САД) - это максимальное давление в артериальной системе, развиваемое во время систолы (сокращения) левого желудочка. Его величина зависит, главным образом, от 1) ударного объема сердца (объема крови, выталкиваемого левым желудочком за одну систолу); 2) эластичности крупных артерий (прежде всего аорты) и 3) объема циркулирующей крови. Верхней границей нормы САД является величина равная 139 мм.рт.ст. Обозначу главные причины по которым САД может превысить нормальные значения: 1) любая физическая или психоэмоциональная нагрузка; речь идет о транзиторном повышении САД под влиянием ситуационного увеличения ударного объема сердца, тахикардии. Например: "гипертония белого халата"; 2) преклонный возраст (старше 65-75 лет); у пожилых лиц аорта из-за возрастного атеросклероза теряет свою "эластичность" (становится жесткой), в результате она перестает выполнять свою амортизирующую функцию (способность растягиваться и сглаживать колебания АД в систолу и диастолу); у пациентов старческого возраста нередко можно обнаружить высокое САД при нормальном или даже пониженном диастолическом ("нижнем") артериальном давлении; 3) гипертоническая болезнь - сопровождается стойким повышением как "верхнего", так и "нижнего" артериального давления. Гипертоническая болезнь по современным представлениям является болезнью неправильного образа жизни. Ее патогенез по-прежнему недостаточно ясен; в основе повышения давления при гипертонической болезни лежит увеличение объема циркулирующей крови и(или) тонуса периферических артерий. Нижней границей нормы САД для подавляющего большинства людей является величина равная 105 мм.рт.ст. (для лиц индивидуально склонных к артериальной гипотонии за нижнюю границу нормы САД принимается значение 90 мм.рт.ст.). Причины низкого САД: 1) первичная гипотоническая болезнь; 2) низкое АД, как индивидуальная норма; 3)при лечении гипертонической болезни - передозировка лекарств; 4) любые шоковые состояния (кардиогенный шок, травматический шок, обезвоживание и т.д.); 5) выраженный системный атеросклероз (у лиц старческого возраста ~ старше 80 лет) - нарушается кровоснабжение мозговых центров регуляции АД.
Диастолическое (нижнее, "почечное") артериальное давление (ДАД) - это минимальное давление в артериях во время диастолы (расслабления) сердца. Его величина зависит от 1) тонуса периферических артерий, 2) эластичности крупных артерий (прежде всего аорты) и 3) "присасывающего" действия аортального клапана. Гемодинамическое влияние указанных факторов приводит к тому, что кровоток становится более или менее равномерным (непрерывным) на протяжении всего сердечного цикла - таким образом во время диастолы поддерживается относительно высокое артериальное давление. Верхней границей нормы ДАД является величина равная 89 мм.рт.ст. Обозначу главные причины по которым ДАД может превысить нормальные значения: 1) гипертоническая болезнь - всегда сопровождается одновременным повышением систолического и диастолического артериального давления, 2) вторичные артериальные гипертонии - особенно высоким ДАД бывает при почечных гипертониях (например 180/140 мм рт ст) - возможно поэтому ДАД иногда называют "почечным". Вообще, чем больше ДАД, тем выше "вклад" в гипертонию спазма периферических артерий. Нижней границей нормы ДАД является величина равная 60 мм.рт.ст. (при индивидуальной склонности к артериальной гипотонии за нижнюю границу нормы ДАД можно принимать значение 50 мм.рт.ст.). Существует несколько основных причин по которым ДАД может быть ниже нормы: 1) выраженный атеросклероз аорты - в основном касается пожилых людей; в такой ситуации склерозированная, уплотненная аорта не способна к растяжению и амортизации при выбросе крови из левого желудочка - итог: диастолическое давление понижается, а систолическое повышается; 2) выраженная аортальная недостаточность - порок сердца, одним из симптомов которого является низкое ДАД; в данном случае пораженный аортальный клапан пропускает кровь обратно в левый желудочек в период диастолы - итог: снижение ДАД из-за "обратного тока" некоторого объема крови в диастолу; 3) выраженная артериальная гипотония - любые причины (передозировка гипотензивных средств, длительный постельный режим, индивидуально низкое АД и т.д.), приводящие к снижению системного артериального давления сопровождаются понижением как САД, так и ДАД.
Диастолическая дисфункция левого желудочка. Нередко в заключении к УЗИ сердца пациенты могут прочитать, о так называемой диастолической дисфункции левого желудочка (ДДЛЖ). Диастолическая функция левого желудочка - это его способность расслабляться после систолы (сокращения); именно в этот период левый желудочек наполняется кровью, затем следует очередное сокращение. ДДЛЖ - невозможность левого желудочка нормально растянуться, расслабиться и адекватно наполниться кровью без "включения" компенсаторных механизмов.
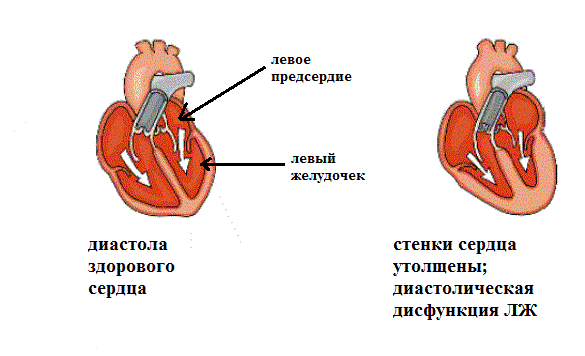
Нарушение диастолической функции ЛЖ приводит к тому, что в левом предсердии (из этой камеры кровь притекает в ЛЖ) начинает повышаться давление за счет застоя в нем крови; в дальнейшем, если ДДЛЖ сохраняется, повышается давление в сосудистой системе легких и т.д.
Способность к нормальному расслаблению камер сердца вообще и левого желудочка в частности, зависит от следующих факторов: жесткости миокарда, давления внутри полости перикарда, частоты сердечного ритма.
- Жесткость миокарда - самая частая причина ДДЛЖ. Любые состояния приводящие к повышению плотности и, соответственно, плохой растяжимости миокарда (преклонный возраст, ожирение, длительная артериальная гипертония, гипертрофия миокарда левого желудочка, некоторые пороки сердца, хроническая ИБС и т.д.), сопровождаются ДДЛЖ.
- Повышение давления внутри полости перикарда. В основном, это относится к неотложной кардиологии, когда по каким-то причинам в полости перикарда скапливается жидкость, которая сдавливает сердце и не дает ему расслабляться. Примеры: ножевое ранение сердца, перикардит (например, при инфаркте миокарда) с выпотом большого количества жидкости, длительные системные заболевания, (онкопроцессы, некоторые ревматические заболевания, уремия и др.)осложняющиеся выпотом в полость перикард. Относительно редкая причина ДДЛЖ.
- Частый ритм сердца. Чем чаще сердце сокращается, тем короче период диастолы (расслабления); соответственно, тем меньшим объемом крови заполниться левый желудочек за столь короткую диастолу - давление в "предшествующих" желудочку камерах будет повышаться. Часто, именно по такому сценарию развивается клиника диастолической сердечной недостаточности у лиц с лишним весом. В таком случае медикаментозное урежение сердечного ритма приводит к нормализации внутрисердечной гемодинамики и уменьшению (купированию) симптомов.
Следует различать понятия ДДЛЖ и диастолической сердечной недостаточности (СН). ДДЛЖ может длительно (годы) протекать бессимптомно, например, при гипертонической болезни. ДДЛЖ, как проявление какого-то патологического состояния, при неадекватном лечении всегда приводит к диастолической СН. Основным и самым первым симптомом диастолической СН является одышка при привычной физической нагрузке. ДДЛЖ надежно диагностируется с помощью УЗИ сердца.
Парасистолия - преждевременное сокращение сердца, которое в отличие от экстрасистолии не зависит от нормального сердечного сокращения, поскольку "не сцеплено" с ним. Другими словами, если экстрасистолия является порождением основного ритма, проявлением чего служит наличие интервала сцепления (появление экстрасистолического сокращения через строго определенные временные промежутки) и подчинение феномену "сверхчастотного подавления", то парасистолия функционирует как самостоятельный, альтернативный водитель сердечного ритма. Парасистолия обладает собственным автоматизмом, который и задает ее частоту. Таким образом, при парасистолии в сердце есть два водителя ритма, не зависящие друг от друга: нормальный (синусовый узел) и эктопический (парасистолический). Если, к примеру, автоматизм парасистолического центра превышает автоматизм синусового узла, то количество парасистол будет превышать количество нормальных сокращений.
На рисунке запечатлены 2 парасистолы: они не связаны (не сцеплены) с основным ритмом, появляются сообразно собственному автоматизму. Если, например, синусовый узел перестанет функционировать (острая блокада синусового узла) - экстрасистолия исчезнет, а парасистолия нет.

Парасистолия, как и экстрасистолия, диагноз сугубо элетрокардиографический. Клиническое значение парасистолии и экстрасистолии схоже. Но есть отличия:
- Соотношение парасистолии и экстрасистолии примерно 1:20 (по моим наблюдением ~1:30-40)
- Парасистолия часто рефрактерна к медикаментозному воздействию, что делает весьма затруднительным ее лечение. Если парасистол очень много, то на помощь приходит методика
РЧА.
- Парасистолия хуже субъективно переноситься, так как она привносит еще больший дисбаланс в нормальную хронологию сердечного ритма, возникая "по собственному велению".
- Очень частая парасистолия приведет к аритмогенной дилатацию сердца с большей вероятностью, чем очень частая экстрасистолия.
- Деполяризация парасистолии определяется кальциевым током, а экстрасистолии - натриевым. Современные антиаритмики эффективно угнетают натриевый ток и слабо - кальциевый.
- На фоне органического заболевания сердца парасистолия более злокачественна, чем экстрасистолия. Другими словами, она чаще чем экстрасистолия вызывает фатальные желудочковые нарушения ритма.
Дефибрилляция - мощный разряд электрического тока, целенаправленно пропускаемый через грудную клетку для нормализации (восстановления) деятельности сердца. Дефибрилляция показана при фибрилляции желудочков или при фибрилляции предсердий. При строгом соблюдении понятийного аппарата дефибрилляция осуществляется только в случае развития клинической смерти, спровоцированной фибрилляцией желудочков. Плановая дефибрилляция, выполняемая для восстановления синусового ритма при фибрилляции предсердий, именуется электроимпульсной терапией. Случаи экстренной дефибрилляции при любых гемодинамически значимых тахиаритмиях, например, осложняющихся шоком или обмороком, называются кардиоверсией.
Суть дефибрилляции при фибрилляции желудочков. Фибрилляция желудочков есть явление абсолютного электрического хаоса в сердце, когда множество волн re-entry циркулируют в толще миокарда по произвольной траектории. Задача дефибрилляции заключается в том, чтобы посредством мощного разряда электрического тока привести значение мембранного потенциала всех клеток сердца к общему знаменателю, как бы "обнулить" электрический заряд сердца. Другими словами, ели при фибрилляции трансмембранный потенциал клеток миокарда имеет хаотичные быстроменяющиеся значения, то после дефибрилляции на какое-то время все клетки будут иметь одинаковое значение мембранного потенциала - это является обязательным условием для того, чтобы активизировался естественный водитель ритм (синусовый узел) и взял под контроль сердечный ритм.
Если не выполнить дефибрилляцию в течение 4 минут, шансы спасти человека в последующем (без явлений декортикации) близки к нулю. За это время электрическая фибрилляторная активность сердца полностью угасает, переходя в редкие агональные сокращения и асистолию. Вот пример дефибрилляции и успешной реанимации человека:
Суть электроимпульсной терапии при фибрилляции предсердий. Смысл манипуляции аналогичен дефибрилляции: "обнулить" трансмембранный потенциал клеток миокарда предсердий, для того, чтобы появились условия для активизации клеток синусового узла. Пример:
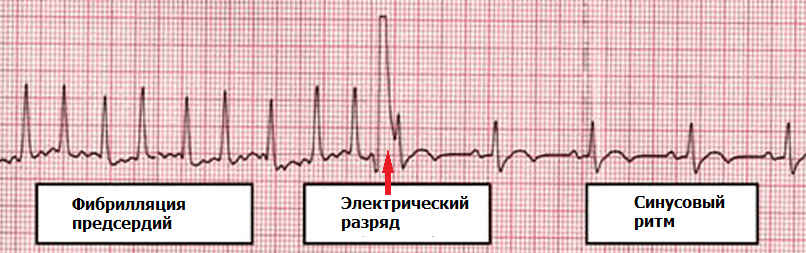
Суть кардиоверсии при тахиаритмиях. Кардиоверсия показана при тех тахиаритмиях, при которых в качестве электрофизиологического механизма выступает macro-reentry. Известно, что macro-reentry имеет так называемое "окно возбудимости" - участок свободный от рефрактерности. Проникая в него, внешний электрический импульс обрывает циркуляцию импульса в миокардиальной петле macro-reentry и прерывает тахикардию:
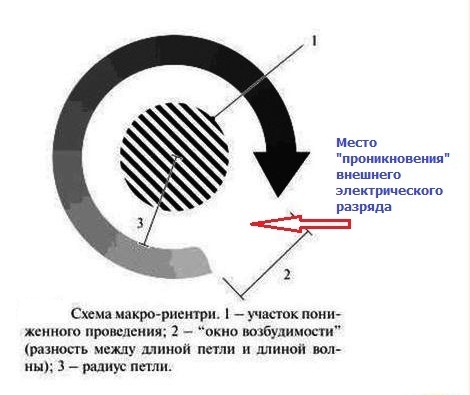
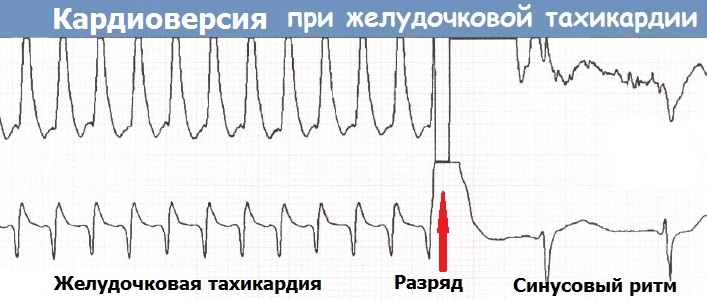
Синусовый ритм - нормальный сердечный ритм человека, когда электрическое возбуждение генерируется в особом участке правого предсердия, называемым синусовым узлом. Синусовый узел представляет собой скопление клеток, способных к спонтанной деполяризации. От синусового узла электрическое возбуждение распространяется на остальной миокарда. Частота синусового ритма (частота сердечных сокращений - ЧСС) в покое колеблется от 60 до 90 в мин. ЧСС менее 60 мин. - называется синусовой брадикардией (это вариант синусового ритма), которая в норме регистрируется в период отдыха, во время сна. ЧСС свыше 90 в мин. - называется синусовой тахикардией (это тоже вариант синусового ритма), которая в норме выявляется при физических и эмоциональных нагрузках, достигая на пике 150-170 сокращений в мин. - согласно потребностям организма.
Двухстворчатый аортальный клапан - врожденный порок сердца, который встречается примерно 1 на 800-1000 человек - то есть не так уж и редко. Аортальный клапан, в норме имеющий 3 створки, в процессе жизни человека испытывает значительные гемодинамические нагрузки - кровь из левого желудочка с силой выбрасывается в аорту, "ударяясь" при этом о ее стенки и раскрывшиеся створки клапана; в период диастолы (расслабления сердца) некоторый объем крови из аорты устремляется обратно в левый желудочек, однако к этому моменту створки аортального клапана оказываются плотно закрытыми, что препятствует ретроградному забросу крови (кровь "сталкивается" с замкнутым клапаном). Нормальный, трехстворчатый аортальный клапан, функционируя в таком режиме "нон-стоп", лишь в преклонном возрасте (старше 60 лет) может подвергаться склеротическим изменениям, кальцификации. Да и то, только в редких случаях его дегенеративная, возрастная инволюция достигает степени порока (сенильный аортальный порок).

Двухстворчатый аортальный клапан является неполноценным. Он подвергается тем же воздействиям, что и трехстворчатый, но имеет на створку меньше. Значит 2 створки будут принимать на себя "нагрузку за троих". Двухстворчатый аортальный клапан значительно легче подвергается инфицированию (бактериальный эндокардит) и гораздо чувствительнее к ревматическому поражению. Но даже если указанные заболевания не развиваются (что чаще и случается у социально адаптированных людей), то двухстворчатый клапан все равно изнашивается (склерозируется) естественным путем значительно раньше трехстворчатого, что проявляется в формировании сердечного порока: аортальной недостаточности. У людей, чья деятельность связана со значительными физическими нагрузками (например, спортсмены), развернутый порок может сформироваться к 40-45 годам; напротив, у лиц далеких от спорта, клиническая картина аортальной недостаточности манифестирует к 55-60 годам. Важно понять, что в любом случае двухстворчатый аортальный клапан приведет к тому или иному осложнению, а значит сократит продолжительность жизни. Самым драматичным исходом вовремя недиагностированного двухстворчатого аортального клапана является внезапная сердечная смерть. Прижизненная диагностика данного порока означает обязательное ограничение интенсивных физических нагрузок (бег, тяжелый фитнесс и т.п.). Если перед нами ребенок, то его лучше направить в жизни по гуманитарному направлению, установив табу на занятие профессиональным спортом. Оперативная коррекция порока проводится по общему кардиохирургическому правилу: протезирование клапана показано тогда, когда польза от его замены заведомо превышает риск самой операции. Другими словами, имплантация клапана предлагается только при появлении значимых симптомов порока - когда в отсутствии операции расчетная продолжительность жизни не превысит 3-5 лет.
Нитроглицерин был выделен в середине 19 века. Изначально это химическое вещество использовалось в технических нуждах, в частности, как взрывчатка. В последующем было установлено, что нитроглицерин является мощным вазодилататором - расслабляет гладкую мускулатуру, присутствующую во многих полых органах и в стенках сосудов. Однако исследователей смущало его короткое время действия ~ 5 минут. Поэтому широкого применения, как спазмолитик он не нашел. Вместе с тем, было выявлено, что нитроглицерин способен быстро и эффективно купировать приступ стенокардии. Данный феномен длительное время объяснялся его прямым вазодилатирующим эффектом - расширением коронарных артерий. Ученые продолжили рациональные изыскания и установили, что сила влияния нитроглицерина на вены и артерии весьма отличается и соотносится примерно, как 10:1. Другими словами, нитроглицерин является прежде всего мощным венозным дилататором, а на артерии значимо действует только в превосходящей концентрации. Постулирование данного феномена озадачило медицинскую общественность, так как необходимо было объяснять его исключительный эффект при приступе стенокардии. В настоящее время доказано, что нитроглицерин купирует стенокардитическую боль через механизм уменьшения сердечной преднагрузки. В физиологии сердечно-сосудистой системы существует понятие преднагрузки и постнагрузки на сердце. Преднагрузка - это весь объем крови, который притекает к сердцу от вен в единицу времени - зависит, прежде всего, от тонуса периферических вен. Постнагрузка - это весь объем крови, который "выталкивает" сердце в артериальное русло в единицу времени - определяется уровнем периферического сопротивления артерий; проще говоря - текущим артериальным давлением. Нитроглицерин, снижая преднагрузку (расширяя вены), способствует депонированию крови в венах, что приводит к уменьшению объема притекаемой к сердцу крови, а значит и к облегчению его работы. В этом и только в этом, заключается его чудодейственность при приступе стенокардии. Другая ниша использования нитроглицерина в кардиологии: купирование явлений острой левожелудочковой недостаточности (отек легких, сердечная астма). При серьезном поражении левого желудочка или его клапанного аппарата (инфаркт миокарда, миокардит, некоторые пороки и др.) возникает застой крови в сосудах легких; вместе с тем, преднагрузка остается на прежнем уровне. Возникает следующая патологическая ситуация: пораженное сердце не в состоянии перекачать весь притекаемый к нему объем крови; кровь начинает застаиваться в сосудах легких, что приводит к отеку легочной паренхимы - так манифестирует сердечная астма, субъективно ощущаемая, как одышка, удушье. Применение нитроглицерина в такой ситуации позволит быстро снизить преднагрузку, что ликвидирует диссонансное соотношение "притока-оттока". Итак, в кардиологии нитроглицерин используется только в 2-х случаях: для купирования стенокардии и явлений левожелудочковой недостаточности. Применение нитроглицерина при любых болевых ощущениях в груди, разумеется, не оправдано. Поскольку нитроглицерин действует не более 5 минут, то, если боль проходит через больший промежуток времени (обычно пациенты говорят: "он снимает боль через 10-20 минут") - значит перед нами какая-то кардиалгия, а боль проходит сама по себе или через эффект плацебо. Учитывая колоссальную распространенность кардиалгий вообще (соотношение кардиалгии и стенокардии при поликлиническом приеме не менее 20:1), то использование нитроглицерина может быть вполне резонно в рамках простого диагностического теста: боль → прием таблетки нитроглицерина → оценка реакции на него в течение ближайших 5 минут. При стенокардии эффект быстрый и полный. В противном случае - это кардиалгия. Если перед нами хроник-сердечник, то отсутствие реакции на нитроглицерин означает 3 возможные клинические ситуации: кардиалгия, затяжной приступ стенокардии (предынфарктное состояние), дебют инфаркта миокарда. Существуют заболевания пищевода, проявляющиеся загрудинными болями весьма похожими по характеристикам на стенокардию, и боль при них может положительно (в том числе быстро) реагировать на нитроглицерин. В такой ситуации только комплексная оценка болевого приступа (появление ее преимущественно в положении лежа, сопутствующие симптомы диспепсии, нормальная ЭКГ на высоте приступа и др.) позволяет исключить ее стенокардитическое происхождение. Основным побочным эффектом нитроглицерина является головная боль. Объясняется она просто: расширяются вены головного мозга → возникает транзиторный микроотек мозговой ткани → появляется ощущение боли в голове. При его хроническом приеме головная боль проходит. Для профилактики приступов стенокардии используются таблетированные формы нитроглицерина длительного действия (до 6-10 часов): Пектрол, Кардикет, Моночинкве и др.

Корвалол - седативное средство, активно используемое в кардиологии для купирования симптомов кардионевроза. Отмечу, что в отличии от других "сердечных" капель, Корвалол имеет в своем составе Фенобарбитал - то есть фармакологическое вещество, обладающее выраженным седативным эффектом. Настойки Валерианы, Пустырника и др. - это просто смесь успокаивающих трав, поэтому не вполне понятно, каким эффектом они обладают: плацебо или лекарственным? Наличие же в Корвалоле Фенобарбитала автоматически классифицирует его, как эффективное успокаивающее средство. Другое дело, что концентрация Фенобарбитала в Корвалоле минимальная, так сказать гомеопатическая. Однако, на мой взгляд, даже такой его ничтожной концентрации достаточно, чтобы в ранге "сердечных" седативных капель он занимал внеконкурентное первое место. Расчет капель Корвалола при приеме его "по требованию" таков: "капля на год жизни". То есть, к примеру, если перед нами 40-летний субъект, то ему следует принять не менее 40-45 капель. Использование Корвалола в меньшей дозировке является одной из главных причин его неэффективности. Больше накапать можно, меньше - в лучшем случае жди плацебо-эффекта. Корвалол и близкие ему средства (Валокардин, Валосердин) применяются в основном для острого снятия кардионевротического симптома: кардиалгия, сердцебиение на фоне тревоги и пр. Некоторые пациенты ссылаются на непереносимость Корвалола из-за наличия в его составе спирта. Я отношусь с пониманием к таким больным. Сейчас в их распоряжении есть масса других нерецептурных седативных средств (Новопассит, Персен и др.), однако их эффективность многими специалистами ставится под сомнение.

Феохромоцитома - опухоль мозгового слоя надпочечников, продуцирующая катехоламины (адреналин, норадреналин). Катехоламины представляют собой адренергические гормоны, синтезирующиеся в парном эндокринном органе - надпочечниках. Катехоламины выделяются в кровь непрерывно в неком базовом количестве для поддержания тонуса симпатической нервной системы (↑артериальное давление, ↑пульс, ↑тонус бронхов и т.д.) . При любых ситуациях, сопровождающихся увеличением физической или эмоциональной нагрузки на организм, катехоламины поступают в кровоток в том количестве, которое необходимо для поддержания текущего гомеостаза. Феохромоцитома - это опухоль целиком состоящая из катехолпродуцирующих клеток. Феохромоцитома чаще поражает один надпочечник, как правило, доброкачественна (не метастазирует); может манифестировать в любом возрасте, однако пик заболеваемости приходится на возрастной диапазон 25-50 лет.
Основным клиническим феноменом феохромоцитомы является неконтролируемый выброс катехоламинов в кровоток, что сопровождается внезапным адренергическим гипертоническим кризом. Его характеристики: скачкообразное повышение артериального давления до высоких цифр (верхнее давление, как правило, превышает 200 мм рт ст), сердцебиение, сильная головная боль, дрожь в теле, потливость, в конце приступа возможны позывы на мочеиспускание или дефекацию. Криз купируется также внезапно, как и возникает. Традиционное медикаментозное лечение, используемое при терапии гипертонической болезни, не предотвращает катехоламиновые кризы при феохромоцитоме - то есть оно абсолютно не эффективно. В межприступный период больной может чувствовать себя здоровым, но если он принимает гипотензивные препараты, то скорей всего артериальное давление будет симптоматично низким. Классическое, кризовое течение феохромоцитомы наблюдается в дебюте заболевания (месяцы или годы); впоследствии, по мере прогрессирования патологии, артериальное давление остается повышенным даже после гипертонического криза. Феохромоцитома, представляя собой синдром вторичной гипертонии, имеет прогредиентное, злокачественное течение неконтролируемой артериальной гипертензии. И если вовремя не проведено радикальное лечение, то один из кризов заканчивается "катехоламиновым шоком" (синдром неуправляемой гемодинамики) и смертью больного. Практически всегда именно врач-кардиолог первым сталкивается с больным с феохромоцитомой, так как высокое артериальное давление это ее единственное проявление. К сожалению, клиническая картина феохромоцитомы может быть стертой: кризы выражены не явно или имеет место стойкое повышение артериального давление, мимикрирующее под обычную гипертоническую болезнь. В такой ситуации врача должна насторожить крайне низкая эффективность профилактической гипотензивной терапии (резистентная гипертония), в том числе при комбинации из 3-4-х препаратов. Диагностируется феохромоцитома лабораторно и инструментально. При обоснованном подозрении на нее сдается анализ крови на свободные метанефрины (метаболиты катехоламинов) - положительный результат с вероятностью 95% будет указывать на феохромоцитому. Визуально данная опухоль диагностируется посредством компьютерной или магнитнорезонансной томографии органов брюшной полости. Если клиника заболевания типична, то этапом лабораторной диагностики можно пренебречь и сразу направить больного на томографию. Лечение заболевания только оперативное (удаление опухоли); перед операцией уже в стационаре больного медикаментозно компенсируют (в течение нескольких дней), стабилизируя АД посредством использования комбинации альфа и бета адреноблокаторов.
Атриовентрикулярные реципрокные тахикардии. В переводе с латинского: атриум - предсердия, вентрикулюм - желудочки. Это группа приступообразных сердечных тахиаритмий, которых объединяет обязательное прохождение (циркуляция) электрического импульса через атриовентрикулярный узел (АВ-узел). Существует 2 основных синдрома, могущие осложниться АВ-тахикардией: феномен WPW и диссоциация АВ-узла. Обе морфологические аномалии имеют врожденный характер, часто, в рамках синдрома дисплазии соединительной ткани. Первая причина - феномен WPW - как уже говорилось выше, представляет собой наличие в сердце дополнительного пути (пучок Кента), с участием которого происходит вращение импульса:
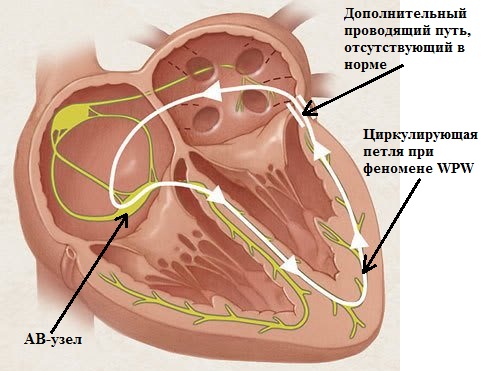
Если петля циркулирует, как на представленном рисунке, против часовой стрелке, то перед нами Атриовентрикулярная ортодромная тахикардия. Слово ортодромность подчеркивает первоначальное прохождение импульса через АВ-узел (антеградно), затем ретроградно (снизу вверх) через проводящий путь на предсердий. Циркуляция импульса в противоположном направлении означает, что сначала он движется антероградно по дополнительному пути, затем ретроградно через АВ-узел на предсердия; такая тахиаритмия называется Атриовентрикулярная антидромная тахикардия.
Вторая причина - диссоциация АВ-узла - то есть разделение АВ-узла на пути с разной скоростью проведения (у здоровых людей АВ-узел гомогенен): упрощенно, на быстрый путь проведения и медленный. В какой-то момент электрический импульс как обычно проводится (сверху вниз, антероградно) по быстрому пути, но не проводится (блокируется) по медленному, однако импульс прошедший по быстрому пути входит в медленный путь с другой стороны (снизу вверх, ретроградно) и вновь проникает в быстрый путь - петля замкнулась, возникает возможность для многократной циркуляции электрического импульса по сформированной петле.
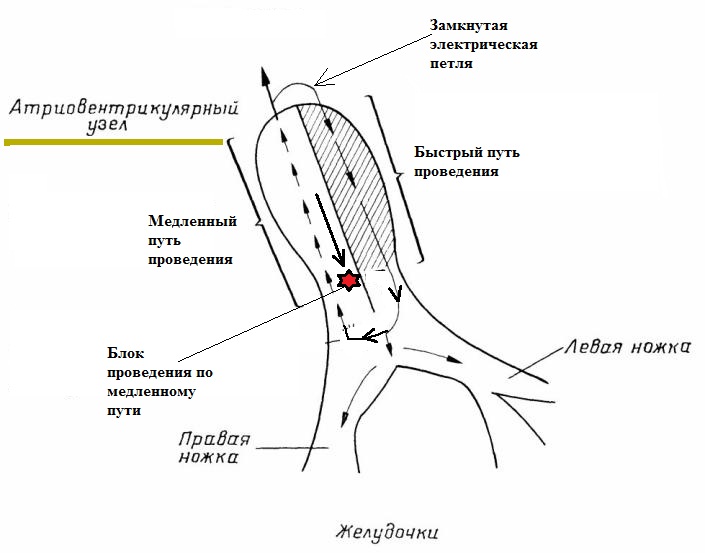
Так запускается Атриовентрикулярная узловая реципрокная тахикардия.
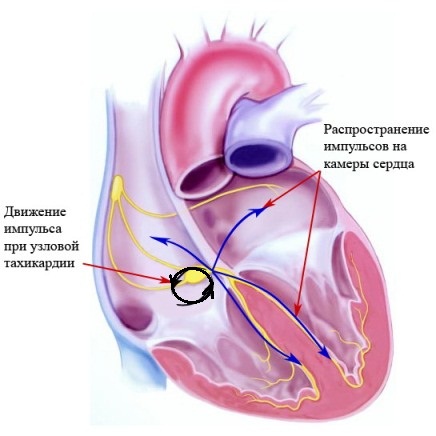 Лица, имеющие
описанные выше врожденные предпосылки для АВ-тахикардии могут быть долгие
годы совершенно здоровы. Признаки феномена WPW
и (или) диссоциации АВ-узла могут выявляться на обычной ЭКГ; однако,
нередко, они отсутствуют, что делает невозможным предвидеть аритмию в
будущем. Как только возникает первый в жизни приступ аритмии, врожденная
аномалия проводящей системы сердца становится болезнью. АВ-тахикардия
представляет собой внезапный пароксизм немотивированного сердцебиения,
запускаемый
предсердной экстрасистолой.
Его частота определяется частотой циркуляции (оборотов) импульса в минуту;
как правило, от 140 до 220 в мин. Для конкретного больного частота
сердцебиения варьирует в незначительных пределах: плюс-минус 10 ударов, а в
течение уже возникшего приступа без постороннего вмешательства частота
остается стабильной на протяжении всего пароксизма. Длительность приступа
может быть совершенно разной: от нескольких секунд, до нескольких часов.
Лечение АВ-тахикардий только оперативное
посредством РЧА. Как правило, к кардиохирургу больной обращается
тогда, когда приступы сердцебиения становятся настолько частыми, что значимо
ухудшают качество жизни. При синдроме WPW
прижигают дополнительный путь, при диссоциации АВ-узла - медленный путь.
Вероятность успеха операции (отсутствие рецидива в долгосрочном периоде)
составляет более 95%. Перед операцией для профилактики пароксизмов
сердцебиения больной может принимать антиаритмическое средство, а
возникающие приступы самостоятельно купировать посредством вагусных проб.
Лица, имеющие
описанные выше врожденные предпосылки для АВ-тахикардии могут быть долгие
годы совершенно здоровы. Признаки феномена WPW
и (или) диссоциации АВ-узла могут выявляться на обычной ЭКГ; однако,
нередко, они отсутствуют, что делает невозможным предвидеть аритмию в
будущем. Как только возникает первый в жизни приступ аритмии, врожденная
аномалия проводящей системы сердца становится болезнью. АВ-тахикардия
представляет собой внезапный пароксизм немотивированного сердцебиения,
запускаемый
предсердной экстрасистолой.
Его частота определяется частотой циркуляции (оборотов) импульса в минуту;
как правило, от 140 до 220 в мин. Для конкретного больного частота
сердцебиения варьирует в незначительных пределах: плюс-минус 10 ударов, а в
течение уже возникшего приступа без постороннего вмешательства частота
остается стабильной на протяжении всего пароксизма. Длительность приступа
может быть совершенно разной: от нескольких секунд, до нескольких часов.
Лечение АВ-тахикардий только оперативное
посредством РЧА. Как правило, к кардиохирургу больной обращается
тогда, когда приступы сердцебиения становятся настолько частыми, что значимо
ухудшают качество жизни. При синдроме WPW
прижигают дополнительный путь, при диссоциации АВ-узла - медленный путь.
Вероятность успеха операции (отсутствие рецидива в долгосрочном периоде)
составляет более 95%. Перед операцией для профилактики пароксизмов
сердцебиения больной может принимать антиаритмическое средство, а
возникающие приступы самостоятельно купировать посредством вагусных проб.
Гипертрофическая кардиомиопатия (ГКМП) - генетически детерминированное заболевание, характеризующееся гипертрофией всего или части миокарда левого желудочка. Встречается 1 случай на 500 новорожденных. Собственно гипертрофические изменения миокарда манифестируют после рождения - чаще всего в подростковом возрасте; однако, развитие гипертрофии может произойти у детей младшего возраста или же, наоборот, у взрослых субъектов (до 30-35 лет). Возможны 3 варианта морфологии ГКМП: симметричная гипертрофия всех стенок ЛЖ, асимметричная гипертрофия межжелудочковой перегородки с незначительной гипертрофией остальных стенок, изолированная асимметричная гипертрофия межжелудочковой перегородки.


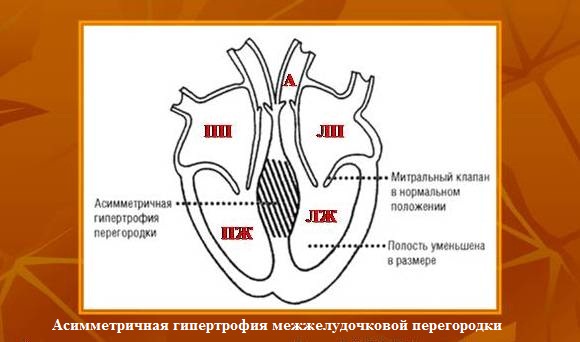
Варианты клинического течения ГКМП: бессимптомное и симптомное. Не менее чем у 1/3 пациентов с ГКМП заболевание протекает скрытно, и человек о нем узнает в лучшем случае при проведении планового УЗИ сердца; а у некоторых диагноз вовсе устанавливается после смерти "от несердечных причин" при вскрытии. Симптомное течение заболевания весьма вариабельно. Самым частым является постепенное развитие сердечной недостаточности через механизм диастолической дисфункции левого желудочка; как правило, симптомы сердечной недостаточности появляются достаточно поздно - на пятом или шестом десятке жизни, прогрессируют медленно. Более редким вариантом течения ГКМП является появление обструктивных обмороков. Причина синкопов лежит в транзиторной обструкции кровотока на уровне выносящего тракта левого желудочка за счет мощной гипертрофии МЖП.
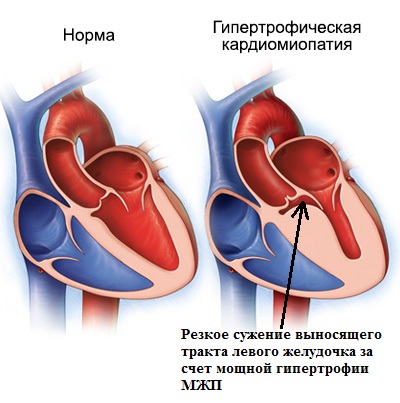 Как
правило, обмороки возникают при физической нагрузке. Данное течение ГКМП
является злокачественным, так любой из обмороков может закончится смертью. К
крайне редкому варианту течения ГКМП относится тромбоэмболический вариант,
как осложнение эндокардита одного из клапанов. Самым драматическим
осложнением ГКМП является
внезапная сердечная смерть
(ВСС). Механизм ВСС - фибрилляция желудочков. Среди причин внезапной смерти
молодых спортсменов ГМКП занимает одно из первых мест. Сама возможность
запуска фатальной желудочковой аритмии при ГКМП заложена в нарушенной
архитектоники гипертрофированного миокарда:
Как
правило, обмороки возникают при физической нагрузке. Данное течение ГКМП
является злокачественным, так любой из обмороков может закончится смертью. К
крайне редкому варианту течения ГКМП относится тромбоэмболический вариант,
как осложнение эндокардита одного из клапанов. Самым драматическим
осложнением ГКМП является
внезапная сердечная смерть
(ВСС). Механизм ВСС - фибрилляция желудочков. Среди причин внезапной смерти
молодых спортсменов ГМКП занимает одно из первых мест. Сама возможность
запуска фатальной желудочковой аритмии при ГКМП заложена в нарушенной
архитектоники гипертрофированного миокарда:
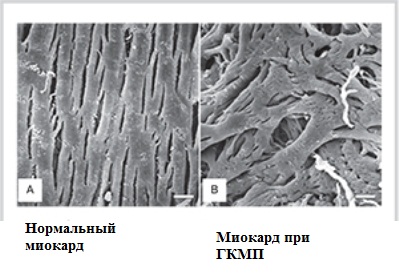 Гистологический
срез здорового миокарда и при ГКМП.
Гистологический
срез здорового миокарда и при ГКМП.
В здоровом миокарде мышечные пучки расположены продольно - это вариант нормы; в миокарде при ГКМП мышечные пучки имеют хаотическую направленность. Такая "рыхлость" миокардиальных волокон предопределяет возможность циркуляции электрического импульса по сложной, непредсказуемой траектории. У всех больных с ГКМП умерших внезапно от острой аритмии, задолго до наступления скоропостижной смерти регистрируется желудочковая экстрасистолия, как единственное проявление электрической "ненормальности" сердца. К сожалению, до сих пор невозможно предвидеть, как клинически будет протекать случайно диагностированная бессимптомная ГКМП. В любом случае, при выставленном диагнозе начать следует с ограничения тяжелых физических нагрузок, исключить профессиональный спорт; и если перед нами ребенок, то направить его в жизни по гуманитарному направлению. Существует несколько предвестников ВСС при ГКМП; каждый из них по отдельности, вероятно, не играет роль предиктора, однако чем их больше у одного больного, тем выше риск аритмической смерти: желудочковая тахикардия при Холтеровсокм мониторировании ЭКГ, необъяснимые обмороки, случаи ВСС у близких родственников, максимальная толщина стенки миокарда ЛЖ более 3 см, парадоксальное снижение артериального давления при физической нагрузке. Пациенты с бессимптомным течением ГКМП нуждаются в пожизненной кардиологической диспансеризации: раз в год УЗИ сердца и Холтер.
Артериальная гипертония беременных. Артериальная гипертония при беременности может протекать в следующих клинических формах:
- Артериальная гипертония, имевшая место до беременности или возникшая в первую половину беременности (до 20 недели); она обычно сохраняется и после родоразрешения. Именуется гипертонической болезнью или, что тоже самое, эссенциальной гипертонией.
- Гестационная артериальная гипертония (гипертония беременных) - индуцирована беременностью, появляется в ее второй половине (после 20 недели). Часто имеет тяжелое течение, осложняется поражением других органов: преэклампсия (нефропатия), эклампсия (нефропатия + отек мозга). В случае, если артериальная гипертония, имевшая место до беременности (гипертоническая болезнь), после 20 недели приобретает злокачественное течение, то также говорят о гестационной гипертонии.
- Неклассифицируемая артериальная гипертония - если гипертония выявляется после 20 недели беременности, однако предыдущие параметры артериального давления неизвестны, то диагностируют гестационную гипертонию. Если после беременности она не проходит, то выставляется диагноз гипертоническая болезнь.
Главной проблемой артериальной гипертонии беременных (в независимости от ее типа) является крайне скудный арсенал терапевтических средств, допустимый к безопасному применению. В связи этим, в США была разработана классификация тератогенности (токсического воздействия на плод) лекарственных препаратов FDA (Foodand Drug Administration):
| Категория | Описание |
|---|---|
| A | Безопасные препараты В контролируемых клинических исследованиях (ККИ) у беременных не выявлено неблагоприятного действия на плод на любом сроке беременности. |
| B | Риск для плода крайне маловероятен. Нет данных о неблагоприятном действии на плод: ККИ у беременных не проводились, но в экспериментах на животных риск для плода не выявлен. |
| C | Риск не может быть исключен, но потенциальная польза приема лекарственного средства (ЛС) может перевесить его возможный вред. ККИ у беременных не проводились. В экспериментах на животных был выявлен риск для плода (особенно в высоких дозах) или эксперименты не проводились. |
| D | Есть доказательства риска неблагоприятного воздействия на плод, но необходимость применения ЛС может превысить потенциальный риск поражения плода (например, когда более безопасные средства неэффективны). Исследования у беременных или данные ретроспективных наблюдений показали возможность тератогенного действия. Эти препараты назначают по жизненным показаниям. |
| X | Препараты с доказанной тератогенностью в эксперименте и клинике. Противопоказаны при беременности. Исследования у людей или животных, а также данные ретроспективных наблюдений показали тератогенное или токсическое действие ЛС на плод, которое, безусловно, перевешивает возможный положительный эффект. |
К гипотензивным средствам из категории А относится только Магнезия, однако внутривенный способ введение ограничивает ее использование в домашних или амбулаторных условиях. К категории В относится Гипотиазид (в дозе до 25 мг/сут.) и Метилдопа (Допегит). Допегит с осторожностью применяют с 16 по 20 неделю беременности, когда возможен тератогенный эффект в отношении нервной ткани плода. В остальное время его использование безопасно, в том числе в высоких дозировках. К категории С относятся следующие гипотензивные препараты: Анаприлин, Нифедипин (простой и ретардный), Каптоприл, Эналаприл, Верапамил, Клофелин, Амлодипин, Бисопролол (Конкор), Метопролол (Эгилок), Небиволол. Данные препараты, когда применяются по строгим показаниям (упорная артериальная гипертония, выраженное сердцебиение), показали свою высокую эффективность и относительную безопасность. Однако, не рекомендуется их длительное использование при беременности в высоких дозах. Гипотензивные средства из группы С желательно не применять в первом триместре беременности, когда идет закладка органов. Если использование все же необходимо, то лучше в малых дозах.
Если артериальная гипертония сохраняется после родоразрешения, то дальнейшая тактика лечения зависит от вида вскармливания. При искусственном вскармливании лечение проводится по общим правилам: ограничений на использование гипотензивных средств нет. При кормлении грудью, необходимо учитывать, что практически все лекарственные препараты попадают в молоко, поэтому подход будет примерно такой же, как при лечении гипертонии во время беременности: опираться следует на классификацию FDA.
Существуют ряд спорных моментов, относительно возможности приема некоторых гипотензивных препаратов. Например, известное гипотензивное мочегонное Индапамид за рубежом относят к категории В по классификации FDA. В России же он считается препаратом группы С, что запрещает его рутинное использование при беременности.
Алкогольная болезнь сердца. Полагаю, вы слышали о способности алкоголя оказывать протективное действие в отношении сердца и сосудов. Суть в следующем... Транспортировка холестерина крови от печени к органами и наоборот (от органов к печени) осуществляется посредством специальных белков. Связка кровяного холестерина и белка называется липопротеидом. Он бывает "хороший" - ЛПВП (липопротеид высокой плотности) и "плохой" ЛПНП - (липопротеид низкой плотности). ЛПВН переносит холестерин от тканей (в частности от сосудов) к печени, где он разрушается - антиатерогенный эффект. ЛПНП, наоборот, транспортируют холестерин от печени к тканям - проатерогенный эффект. Было установлено, что регулярное (ежесуточное) употребление небольших доз алкоголя (50 мл водки, коньяка или 200 мл красного вина) достоверно повышает концентрацию ЛПВП, что приводит к "оттоку" холестерина из стенок сосудов и препятствует развитию атеросклероза. Этот феномен назвали "французским парадоксом", поскольку было замечено, что французы - любители красного вина - оказывались резистентными к атеросклерозу. Однако "какой же русский ограничится рюмкой водки!?" Поэтому практических рекомендаций по употреблению алкоголя с целью "лечения сердца" в медицинской литературе вы не найдете. Если же вы равнодушны к алкоголю и всегда знаете меру, то вполне можете себе позволить употреблять указанную дозу для "чистки сосудов" и будьте уверены: это полезно. Для большинства людей алкоголь является способом релаксации после тяжелого рабочего дня, возможностью снять внутреннее напряжение для "связки разговора" в компаниях, уходом от экзистенциальной неудовлетворенности - одним словом: допингом. Можно представить в каком количестве он употребляется в таких ситуациях. С другой стороны, трудно встретить человека, который целенаправленно избегает алкоголя - это либо алкоголик, проходящий лечение, либо перфекционист. Употребление алкоголя в знакомой доброй компании, особенно, если речь идет о редких эксцессах (пусть будет не чаще раз в месяц), приносит известное удовлетворение от коммуникации, задушевных разговоров. В таком случае психологический выхлоп от полученных положительных эмоций может перекрывать негативное воздействие на организм от однократно превышенной дозы алкоголя. Что касается бытовых пьяниц и алкоголиков, то у них прежде всего поражается нервная система (изменение личности) и печень (жировая дистрофия и, как крайнее проявление, цирроз печени). Поражение сердца, возможно, встречается у алкоголиков тоже часто, однако степени клинической значимости алкогольное заболевание миокарда достигает относительно редко. Речь идет о так называемой алкогольной кардиомиопатии. Выраженность симптомов при этом заболевании может варьировать от просто "плохой ЭКГ" и безобидных болей в области сердца (частый вариант), до тяжелой сердечной недостаточности, быстро приводящей к смерти (редкий вариант). Кроме того, любители спиртных напитков часто заболевают артериальной гипертонией и пароксизмальной мерцательной аритмией.
Эстрогены в кардиологии. Общеизвестно, что женщины заболевают атеросклерозом позже мужчин, что принято объяснять протективной ролью эстрогенов в отношении сосудистой стенки. Вместе с тем, "потоковое" назначение эстрогенов всем женщинам с естественной или хирургической менопаузой не приводит к достоверному снижению риска заболеваемости атеросклеротическим заболеванием (ИБС, ишемическая болезнь головного мозга). Было сформулировано понятие "терапевтического окна" в заместительной гормональной терапии (ЗГТ) для протекции органов сердечно-сосудистой системы. Доказано, что назначение эстрогенов не позже 7-8 лет, от момента наступившей менопаузы, способно снизить сосудистые риски. То есть лицам старше 58-60 лет ЗГТ бессмысленна или даже опасна, так имеются сведения о повышении вероятности тромбообразования у них. Принципы ЗГТ у женщин для снижения сосудистых рисков:
- ЗГТ имеет смысл назначать не позже 8 лет от начала менопаузы,
- при назначении ЗГТ лучший эффект наблюдается у женщин, чей индекс массы тела не превышает 30 кг/м²,
- целесообразно парентеральное введение эстрогенов (гели, пластыри, вагинальные кремы или свечи, подкожные имплантаты),
- при назначении ЗГТ опираются на наличие раннего атеросклеротического заболевания, неблагоприятной наследственности (ранняя заболеваемость у матери) или атерогенной дислипидемии (высокий уровень ЛПНП и низкий уровень ЛПВП); назначение ЗГТ всем женщинам не оправданно и даже, скорее, опасно,
- эстрогены при ЗГТ назначаются в низких или ультранизких дозировках,
- продолжительность ЗГТ не должна превышать 8-10 лет; другими словами, если менопауза (климакс) наступила в 50 лет, а ЗГТ по кардиологическим показаниям назначается в 55 лет, то в 58-60 лет она должна быть обязательна прекращена.
Смысл ЗГТ в кардиологии заключается в том, чтобы "мягко", без последствий перейти к естественному менопаузальному периоду жизни женщины.
Деменция - значительное снижение умственных способностей (в простонародье: слабоумие), возникшее вследствие приобретенного органического поражения головного мозга. По статистике после 90 лет деменцией страдает около 60% человек. Причин для деменции множество. Однако у кардиологических больных значительно преобладает две: болезнь Альцгеймера и сосудистая деменция. Основные ранние клинические проявления деменции: снижение памяти (забывчивость), изменение социальной активности, утрата интереса к хобби, снижение мотивации, уменьшение способности к обучению, снижение внимания, уменьшение выразительности речи, пренебрежение гигиеной. Болезнь Альцгеймера в абсолютном большинстве случаев дебютирует после 65 лет; течение медленное, неуклонно-прогрессирующее. Сосудистая деменция - возникает на фоне атеросклероза артерий головного мозга. Она (сосудистая деменция) может нарастать постепенно, например, на фоне нелеченной артериальной гипертонии или возникнуть внезапно, например, после перенесенного инсульта. Объединяет болезнь Альцгеймера и сосудистую деменцию то, что борьба с факторами риска раннего старения сосудов значительно снижает вероятность заболеть одним из этих заболеваний. Корригируемые факторы риска: артериальная гипертония, курение, повышенные липиды крови, сахарный диабет, гиподинамия, избыточный вес, одиночество, низкий уровень общей культуры. Некоррегируемый фактор риска: сам преклонный возраст. В запущенных случаях деменция заканчивается психическим и физическим маразмом.
Псевдогипертензия - феномен ложнозавышенных цифр артериального давления, встречающийся у лиц преклонного возраста. В основе псевдогипертензии лежит выраженный возрастной артериосклероз (уплотнение артерий), в результате которого манжета тонометра способна пережать плечевую артерию только при значительном нагнетании в нее воздуха - цифры АД на циферблате будут заведомо превышать фактическое артериальное давление. Разница между измеренным и реальным АД может составлять 30-40 и более мм рт ст. Подумать о псевдогипертензии следует тогда, когда стойко высокие цифры АД не коррелируют с клинической симптоматикой (хорошее самочувствие, отсутствие выраженной гипертрофии миокарда левого желудочка). Иногда выявить псевдогипертензию позволяет прием Ослера: производят накачивание измерительной манжеты, наложенной вокруг плеча, выше систолического давления, и тщательно пальпируют лучевую и/или плечевую артерии. Если одна из этих артерий явно пальпируется как плотная трубка, несмотря на отсутствие пульсации во время накачивания манжеты, больной является Ослер-положительным, имеющим ложноповышенные показатели САД или ДАД. Нередко у лиц с псевдогипертензией во время проведения теста артерию прощупать не удается (например, у полных субъектов), что делает невозможным доказать или опровергнуть наличие ложнозавышенного АД; в таком случае истинные цифры АД можно узнать только инвазивно (интраартериально). В целом, следует помнить, что феномен псевдогипертензии встречается сравнительно редко, даже у лиц старческого возраста.
Постпрандиальная артериальная гипотония - физиологическое снижение артериального давления на 5-10 мм рт ст после приема пищи. В норме человек не ощущает постпрандиальной гипотонической реакции в силу незначительного снижения цифр АД. В худшем случае мы испытываем легкую транзиторную вялость и сонливость. У лиц с вегетативной недостаточностью постпрандиальная артериальная гипотония может быть выраженной (↓ АД на 20-40 мм рт ст), что сопровождается слабостью (вплоть до полуобморочного состояния), рефлекторным сердцебиением. Выход только один: прием пищи малыми порциями.
Невропатия (невропатический тип личности) - врожденная (конституциональная) особенность нервной системы, которая характеризуется тревожно-мнительной или тревожно-фобической аномалией личности. Иногда невропатия формируется уже в зрелом возрасте под влиянием пережитого стресса высокой личностной значимости. Такие субъекты склонны 1) к гиперстезии в сфере телесных ощущений (разнообразные болевые ощущения, порой, мигрирующего характера), 2) к полиморфным вегетативным дисфункциям (эпизоды гипотонии/гипертонии, вазовагальные обмороки, панические атаки, головокружения, тенденция к синусовой тахикардии, потливость ладоней и др.), 3) к нарушению в сфере эмоций (чрезмерная акцентуация на собственном здоровье, высокий уровень личностной тревожности, разнообразные фобии). Пациенты с невропатическим типом личности, в зависимости от преобладания той или иной симптоматики, "мигрируют" между врачами трех специальностей - кардиологом, неврологом и психотерапевтом. Обследование соматического статуса у таких субъектов не выявляет изменений внутренних органов.
Миграция водителя ритма по предсердиям - особенность сердечного ритма, когда первоисточник, генерирующий электрически импульс, исходит из разных отделов предсердий. В какой-то степени это устаревшая трактовка данного ЭКГ-синдрома. По современным представлениям водитель ритма "мигрирует" в пределах синусового узла, который у таких субъектов имеет вытянутую форму, достигая фиброзного кольца сердца.
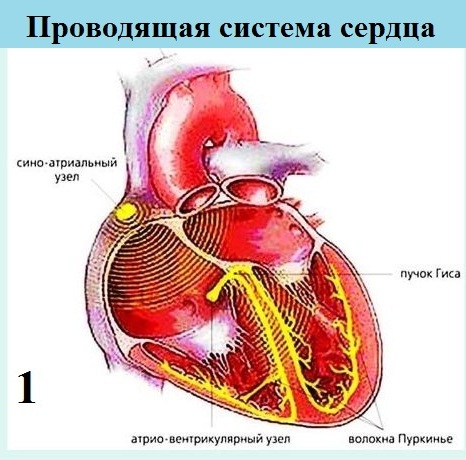

Обратите внимание на рисунок 1: перед вами гистологический срез "нормальной" проводящей системы сердца. Синусовый узел располагается "на крыше" правого предсердия возле верхней полой вены, имеет округлую форму. Теперь внимательно посмотрите на рисунок 2: синусовый узел имеет удлиненную форму, "распространяясь" вниз - вдоль латеральной стенки правого предсердия - до "нижней полой вены. Именно так выглядит синусовый узел у субъектов с ЭКГ-проявлениями миграции водителя ритма по предсердиям. То есть первый импульс генерируется в верхней части синусового узла, а последующие исходят из все более дистально расположенных участков синусового узла; последний импульс формируется в самой нижней его части. Затем цикл "миграции" импульса по предсердиям (точнее: по синусовому узлу) повторяется. Это абсолютно безобидная ЭКГ-аномалия! Чаше встречается у лиц с дисплазией соединительной ткани и при невропатии.
Соматизированная депрессия/тревога. На страницах сайта я неоднократно упоминал, что когнитивные невротические симптомы могут "маскироваться" под соматические ощущения. Другими словами, невроз может представляться (субъективно восприниматься) больным как некий телесный недуг. Более того, именно данные ощущения, порой, служат поводом для обращения к врачу. А симптомы бывают самые разнообразные: сердцебиение; боли в области сердца с иррадиацией в лопатку, левую руку; перебои в работе сердца; лабильность артериального давления. Собственно невротические/психотические симптомы в такой ситуации объективно транслируются неким фоном, не осознаваемым больным как патологический недуг, например: депрессия или тревога. Соматизированная депрессия/тревога - "мимикрия" невроза под соматическое заболевание. Сами же невротические симптомы - тревоги и/или депрессии - верифицируется только при детализированном опросе.
Кардиальный синдром Х - симптомокомплекс, при котором клинические проявления загрудинного болевого синдрома соответствуют проявлениям типичной стенокардии (за исключением положительного эффекта на нитраты), но коронарные артерии остаются интактными (не имеют концентрических атеросклеротических бляшек по данным коронарографии). Клинические характеристики синдрома:
- соотношение женщин и мужчин 10:1,
- чаще всего встречается в зрелом возрасте (от 40 до 65 лет),
- нередко такие пациенты имеют лишний вес, нарушение толерантности к глюкозе (или сахарный диабет), тенденцию к синусовой тахикардии и гипервентиляционный синдром. Либо 2-3 признака из перечисленных.
Общепринятой концепции патогенеза кардиального синдрома Х нет. Раньше считалось, что в его основе лежит воспалительное поражение коронарных артериол (мелких артерий, не визуализируемых при коронарографии) и, как следствие, возникновение ишемии при физической нагрузке. В настоящий момент эта теория подвергается обоснованной критике, прежде всего, вследствие противоречивости и недоказуемости.
Современные концепции кардиального синдрома Х:
1) У лиц с избыточной массой тела проявление данного синдрома может быть следствием относительной коронарной недостаточности на фоне диастолической дисфункции (ДД) и гипертрофии миокарда (ГМ) левого желудочка (ЛЖ). Субъекты с висцеральным ожирением практически всегда имеют и то (ДД), и другое (ГМЛЖ). Существует предположение о дополнительной патогенетической роли дисфункции эндотелия, ассоциированного с дефицитом выброса в кровь естественного вазодилататора - оксида азота (NO).
Таким образом, кардиальный синдром Х может возникнуть при сочетании выше упомянутых предпосылок. Дисфункция эндотелия в этом ряду стоит облигатным фактором, поскольку в нормальных условиях физическая нагрузка сопровождается выбросом в кровь NO и расширением артерий сердца. Лишний вес является независимым фактором риска развития ДДЛЖ. При тахикардии на фоне физической нагрузке усиление диастолической дисфункции ЛЖ приводит к относительной коронарной недостаточности транзиторного характера. Напомню, что основное кровенаполнение миокарда осуществляется в диастолу. Ее неполноценность (дисфункция/укорочение за счет повышенной "жесткости" миокарда левого желудочка) может быть причиной появления ангинозоподобной боли при нагрузках.
В отличие от вторичной стенокардии при кардиальном синдроме Х гипертрофия сердца никогда не бывает выраженной. Образно говоря, на "единицу" миокардиальной ткани приходится адекватное количество коронарных артериол - в этом принципиальное отличие вторичной стенокардии от синдрома Х.
2) Частой клинической находкой при кардиальном синдроме Х является наличие тревожного расстройства и одного из его проявлений - гипервентиляционного синдрома, который, к слову, относится к типичному невротическому симптому. "Дыхательное поведение", усиливающееся или провоцирующееся физической нагрузкой, способствует развитию дыхательного алкалоза (ощелачиванию крови). Само по себе снижение РН крови может проявляться общей дурнотой, головокружением, распирающими болями в груди. В большинстве случаев болевой синдром, возникающий при данном патогенетическом варианте развития синдрома Х, возникает и вне физической нагрузки - в любой ситуации, когда появляется "дыхательное поведение".
Лечение кардиального синдрома Х исключительно терапевтическое и подбирается исходя из вероятного ведущего механизма патогенеза. Нередко терапия малоэффективна, что вынуждает пациента пребывать в состоянии "врачебного шоппинга". Прогноз - благоприятный.
Внезапная сильная потливость. Несмотря на неспецифичность данного симптома, в большинстве случаев он возникает в ситуациях, которые пациентом субъективно воспринимаются как опасные или являются таковыми объективно. Лейтмотивом внезапной сильной потливости является мощная, стремительная и недифференцированная активация симпатической нервной системы (СНС). Каковы физиологические эффекты данного феномена? Перечислим некоторые кардиальные: централизация кровообращения (усиление кровоснабжения в жизненно важных органов в ущерб другим) за счет спазма периферических артерий, учащение дыхания, сердцебиение. Сильная внезапная потливость есть одно из следствий недифференцированной гиперактивации симпатической нервной системы. Какие ситуации могут провоцировать данный эффект?
- любая сильная боль (например, при развитии инфаркта миокарда),
- сильный страх,
- быстрое снижение давления, которое по определению сопровождается компенсаторной активацией СНС и централизацией кровообращения.
В условиях клинической медицины данный симптом может быть составной частью доброкачественного феномена (например, вазовагального обморока) или являться одним из проявлений ургентного шокового состояния.