Лечение и реабилитация больного с инфарктом миокарда в условиях стационара является сложной и ответственной задачей. То внимание, которое уделяют госпитальные врачи "инфарктным" пациентам, к сожалению, не всегда совпадает с тем, какое внимание им уделяется амбулаторным медицинским звеном после выписки из больницы. И главное: сами больные далеко не всегда мотивированы на фундаментальный анализ и осознание пережитой "катастрофы". Вместе с тем, жизнь после инфаркта миокарда должна быть переосмыслена и в какой-то степени разделена на "до" и "после".

Базовый вопрос, который пациент с перенесенным инфарктом должен задать себе звучит так: почему заболел именно я? Ответ на него является отправной точкой не только для последующего лечения, но и всей дальнейшей жизни заболевшего. Если пациент не ставит перед собой такого вопроса или вообще игнорирует факт перенесенного заболевания (отношение к болезни: "это случилось не со мной"), то обязательно будет второй инфаркт миокарда (скорее, смертельный или, как минимум, с глубоко инвалидизирующими последствиями). Понимая, что пациент с инфарктом миокарда может быть совершенно далек от медицины, вопрос о происхождении заболевания должен формулироваться его лечащим поликлиническим врачом сразу после выписки из стационара.
Перед тем как перейти к основной части разговора, считаю необходимым остановиться на одном важном аспекте. Как относиться к инфаркту миокарда в старости? Известно, что преклонный возраст сам по себе является мощным фактором риска любого атеросклеротического заболевания, включая ишемическую болезнь сердца и одного из ее проявлений - инфаркта миокарда. Однако объяснять "старческий инфаркт" исключительно возрастной инволюцией сосудов можно, вероятно, только в очень преклонном возрасте. Возьму на себя смелость и обозначу этот возрастной рубеж: от 80 лет и старше. Итак, только в глубокой старости инфаркт миокарда следует считать естественным проявлением увядания, умирания организма.
Примерно в 95-98% случаев субстратом для развития инфаркта миокарда служит атеросклероз артерий сердца. Во внутренней оболочке (эндотелии) крупных сердечных артерий происходит отложение липидов (преимущественно холестерина). Формирующаяся атеросклеротическая бляшка выступает в просвет артерии, сужая его. Надрыв бляшки запускает процесс агрегации тромбоцитов и формирование тромба, полностью или частично окклюзирующего просвет сосуда. "Экзотические" причины развития инфаркта миокарда, например: из-за врожденной аномалии развития коронарых артерий, воспаления коронарных сосудов (коронариты), миокардита с исходом в крупноочаговый кардиосклероз, расслаивающей аневризмы аорты - встречаются исключительно редко.
Итак, если человек перенес инфаркт миокарда, то подразумевается, что у него имеется атеросклероз сердечных артерий. В таком случае выяснение причины инфаркта автоматически сводится к разговору о происхождении атеросклероза. Факторы риска атеросклероза можно разделить на липидные и нелипидные.
К нелипидным факторам риска коронарного атеросклероза относятся те, которые не ассоциируются с повышенным уровнем кровяного холестерина. Несмотря на то, что "без холестерина - нет атеросклероза", далеко не всегда при манифестированном атеросклерозе диагностируется дислипидемия (гиперхолестеринемия). Предполагается, что при "нелипидном пути" атеросклероза происходит активное перикисное окисление липидов крови. А перикисно-окисленные липиды крайне атерогенны: они начинают инфильтрировать стенку артерий даже, если их концентрация формально не выходит за пределы установленной нормы. Что же это за нелипидные факторы риска?
1. Определенная поведенческая психодинамика (хронический стресс). Выделяют два, в какой-то степени противоположных, типа поведения, предрасполагающих к коронарному атеросклерозу:
- Принцип ключевого (сверхценного) переживания. Характерен для лиц с высокой социальной активностью, наделенных нарциссическими качествами, эмоционально ригидных, бескомпромиссных, настроенных на максимальный объем достижений при объективно низком контроле и недоверии по отношении к другим. Возможные варианты ключевого переживания: обвинения в несостоятельности (или недооценка) профессиональных достижений, невозможность выполнить принятые на себя обязательства, угроза деловой репутации, неизбежность расставания (потери). Негативное разрешение ключевого переживания воспринимается, как грубая нарциссическая обида с эмоционально-депрессивной окраской ("крушение всех надежд"). Несмотря на то, что сверхценное переживание относится к нелипидному фактору риска, при данном паттерне поведения дислипидемия является частой находкой. (Личность типа А)
- Принцип конверсии. Тревожно-депрессивный характер в сочетании с трудностью в выражении эмоций и попыткой их скрыть, быстрая психическая истощаемость, низкая социальная поддержка, зависимое положение, тенденция к избегающему поведению. (Личность типа D). Преобладает среди лиц с невысоким социальным статусом.
2. Пожилой возраст. К коронарному атеросклерозу предрасполагает не старение в общебиологическом смысле, а те подсознательные процессы, которые могут сопровождать человека в старости. Психодинамика коронарного атеросклероза в старости: субдепрессивность в связи с потерей ранговости (социальной или внутрисемейной), одиночество ("синдром опустошенного гнезда"), экзистенциальный вакуум (неосознаваемое отсутствие смысла жизни). В целом психодинамика схожа с выше описанным принципом конверсии.
3. Курение. Никотин активизирует симпатическую нервную систему, что приводит к повышению артериального давления, учащению сердечного ритма и как следствие - "изнашиваемости" эндотелия (внутренней оболочки артерий). Крайне патогенными являются ситуации, когда "коронарная" поведенческая психодинамика сочетается с курением.
4. Неконтролируемая артериальная гипертония. Высокое кровяное давление гемодинамически травмирует артериальный эндотелий, что приводит к транспортировке в зону "повреждения" строительного материала - холестерина. В целом психодинамика гипертонической болезни схожа с таковой при коронарном атеросклерозе, однако в последнем случае подсознательно "на кон" ставится больше, поэтому возникающие проблемы субъективно воспринимаются еще драматичнее. Зачастую, пациент так погружен в пучину жизненных событий, что не ощущает артериальной гипертензии, которая может протекать в рамках "гипертонии на рабочем месте".
Теперь рассмотрим самые распространенные липидные факторы риска коронарного атеросклероза, при которых в анализе крови выявляется тот или иной вид дислипидемии. В таком случае липиды крови способны инфильтрировать стенку артерии по принципу градиента концентрации.
1. Гиперхолестеринемия или дислипидемия. При первичной гиперхолестеринемии имеет место врожденное нарушение метаболизма холестерина. Встречается очень редко: ~ 1 человек на 1000. Заподозрить ее можно, когда беспричинно уровень кровяного холестерина превышает значение 10-11 ммоль/л. Вторичная гиперхолестеринемия - весьма распространенное явление, тесно ассоциированное с неправильным режимом питания (перееданием) и лишним весом.
2. Сахарный диабет. Некорректно леченный сахарный диабет обязательно сопровождается дислипидемией. Крайне важно, чтобы компенсация сахарного диабета была максимально полной. Субкомпенсация, когда глюкоза крови натощак находится в пределах 7-9 ммоль/л, приравнивается к некорректно леченному сахарному диабету. Во всяком случае, дислипидемия на таком фоне будет обязательно.
3. Ожирение. Речь идет не просто об избыточной массе тела, а о превышении индекса массы тела (ИМТ = масса тела в кг / (рост в метрах)²) значения 30. Ожирение обязательно ассоциируется с перееданием, вторичной гиперхолестеринемией и малоподвижным образом жизни.
Итак, больной с перенесенным инфарктом миокарда должен знать о своем факторе риска, который в его конкретном случае послужил причиной заболевания. Поскольку психодинамические "прединфарктные" процессы протекают в подсознательной сфере, наиболее сложным для больного является осознание и признание именно психодинамики заболевания.
Жизнь после перенесенного инфаркта миокарда должна начаться с упразднения факторов риска. Если это не будет сделано, то случится повторный инфаркт. Очевидно, что посильную помощь должны оказать родственники. От них зависит та психологическая обстановка, в которой больному предстоит "экзистенциальная реабилитация". Возможно для полновесной коррекции образа жизни потребуется помощь других врачей: нарколога, диетолога, эндокринолога, психотерапевта.
Отсутствие борьбы с факторами риска - большая ошибка. Некоторые российские кардиологи даже дали название такому феномену - "русский парадокс" - борьба не с причиной инфаркта миокарда, а с его последствиями.
Следующий вопрос, который должен задать себе больной после перенесенного инфаркта миокарда: какой объем физической нагрузки допустимо выполнять? Ответ на него гораздо сложнее, чем кажется на первый взгляд. Для начала в качестве постулата следует принять следующее утверждение: в течение месяца после инфаркта миокарда необходимо избегать любых сверхнагрузок. Причем месяц лучше отсчитать с момента окончания госпитализации. Максимально допустимой нагрузкой в это время будут пешие уличные прогулки. За этот месяц на месте инфарцированного миокарда сформируется полноценный соединительнотканный рубец.
Ответ на поставленный вопрос зависит от нескольких факторов:
1. Какой инфаркт миокарда был перенесен: крупноочаговый (трансмуральный, Q-позитивный) или мелкоочаговый (субэндокардиальный, Q-негативный)?
2. Была ли "открыта" (стентирована) инфаркт-зависимая артерия?
3. Есть ли гемодинамически значимые сужения в других артериях (от 75-80% и больше)?
4. Если инфаркт крупноочаговый, то визуализируется ли рубец при УЗИ сердца, выполненном в стационаре?
5. Если инфаркт крупноочаговый, то визуализируется ли рубец при УЗИ сердца в динамике (через 1-6-12 месяцев после инфаркта)?
Ответ на первые на 4 вопроса можно получить от своего лечащего врача или прочитать в выписном эпикризе; на 5-й вопрос вам ответит врач-УЗИст, выполняющий исследование в динамике.
Первая ситуация. Пациент перенес мелкоочаговый инфаркт миокарда или абортированный крупноочаговый (не видимый при УЗИ); инфаркт-зависимая артерия стентирована; в других артериях сужений нет. После месячной реабилитации допустима любая физическая нагрузка. Другими словами, в плане физической активности жить можно как прежде: ограничений нет.
Вторая ситуация. Пациент перенес мелкоочаговый инфаркт миокарда или абортированный крупноочаговый (не видимый при УЗИ); стентирована инфаркт-зависимая артерия; в других(ой) артериях(ии) имеются гемодинамически значимые сужения. До тех пор пока сохраняются значимые сужения в других артериях - должны быть исключены сверхнагрузки. Допустима физическая активность следующего плана: ходьба не выше среднего темпа, дачные работы, работы по дому, легкие аэробные физические нагрузки без выраженной одышки. Как только в результате плановой кардиохирургической операции (стентирование или шунтирование) все сердечные артерии будут "открыты", любые ограничения на физическую нагрузку снимаются.
Третья ситуация. Пациент перенес крупноочаговый инфаркт миокарда, доказанный при выполнении УЗИ сердца в стационаре. Однако в динамике, при повторных УЗИ сердца, проводимых уже на поликлиническом этапе, "рубец" не виден. Подобное встречается нередко. Объясняется это тем, что хоть инфаркт и случился через всю толщу миокарда, но он был небольшим по площади ("в ширину"). В процессе репарации миокард компенсаторно гипертрофировался вокруг рубца и тем самым как бы его "замаскировал". Если у такого пациента инфаркт-зависимая артерия стентирована, а остальные артерии проходимы, то ограничения будут распространяться только на интенсивные физические нагрузки, сопровождающиеся выраженной одышкой (бег, тяжелый фитнесс, ходьба в горку быстрым шагом). Если же имеются гемодинамически значимые сужения в других артериях, ограничения более существенны: допустимы только те нагрузки, которые не будут сопровождаться одышкой. И так до тех пор, пока хирургически не "откроют" суженные артерии.
Четвертая ситуация. Пациент перенес крупноочаговый инфаркт миокарда, доказанный при выполнении УЗИ сердца в стационаре; инфаркт-зависимая артерия стентирована. Рубец визуализируется и при всех последующих УЗИ сердца. Даже несмотря на то, что после выписки такой пациент может себя чувствовать субъективно здоровым, у него имеется очень высокий риск внезапной сердечной смерти. Чтобы свести его к минимуму необходимо пожизненно исключить сверхнагрузки. Нагрузки средней интенсивности (уборка снега, быстрая ходьба, ношение тяжестей и т.п.) допустимы, но весьма дозированно. Основная причина по которой пациенты из этой группы оказываются повторно стационированы: превышение допустимой нагрузки на сердце. Происходит буквально следующее: в левый желудочек притекает больше крови, чем он в состоянии выбросить ее в артериальное русло из-за своей "слабости" (недостаточности). При соблюдении приемлемого режима физической активности приток и отток будут эквивалентны. В данном случае не имеет значение состояние других коронарных артерий. Главное: в левом желудочке имеется обширный рубец, который является субстратом для систолической сердечной недостаточности. Игнорирование заболевания приведет либо к внезапной смерти за счет фибрилляции желудочков, либо к приступу сердечной астмы с последующей госпитализацией.
Пятая ситуация. Пациент перенес мелкоочаговый или крупноочаговый инфаркт миокарда, однако по каким-то причинам инфаркт-зависимая артерия не была открыта (стентирована). Это самая опасная ситуация, так как сохраняется субстрат заболевания: окклюзированная артерия. Особенно высок риск внезапной сердечной смерти. До тех пор пока артерия не будет открыта допускаются только легкие аэробные физические нагрузки: ходьба по улице небыстрым шагом, легкие домашние работы. Если операция не показана (например, крайне высокий риск смерти при проведении АКШ у пожилого пациента), то подобный формат нагрузки сохраняется до конца жизни.
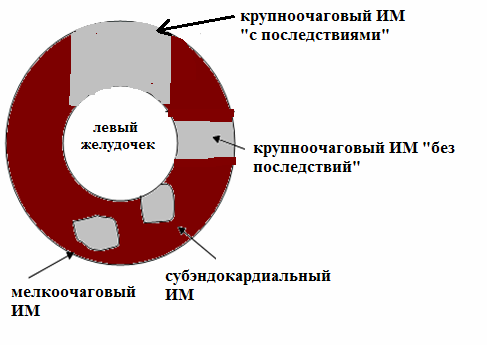
Конечно, описанные выше клинические ситуации предельно упрощены; показаны наиболее типичные случаи. В реальности встречаются разные нюансы, влияющие как на лечебную тактику, так и на программу физической реабилитации. Например, инфаркт миокарда на "чистых" артериях (редко, но бывает); гемодинамически значимое сужение в проксимальном (крупном) сегменте артерии гораздо опаснее такого же сужения в дистальном (мелком) сегменте; повторный инфаркт миокарда; инфаркт миокарда в глубокой старости и др. Тем не менее, моей задачей было указать некий ориентир.
Превышение допустимой интенсивности физических нагрузок постинфарктным больным является основной причиной внезапной сердечной смерти вне стационара.
Чтобы увидеть воочию разницу между инфарктом миокарда "с последствиями" и "без последствий" рекомендую просмотреть 2 коротких видеофайлы (не забудьте включить кнопку "повтор" на видеоплейере): инфаркт "с последствиями", инфаркт "без последствий".
Следующий вопрос, который задает себе больной после перенесенного инфаркта миокарда: какие лекарственные препараты я должен принимать? Существует некий минимальный набор медикаментов, которые рекомендуется пожизненно принимать каждому постинфарктному пациенту: антиагрегант, статин, бета-блокатор, ингибитор АПФ. Однако здесь также следует ориентироваться не на "клинические постулаты", а на конкретного больного.
Стентирована ли у больного коронарная артерия? Если да, то в течение минимум 12 месяцев пациенту необходимо принимать двойную антиагрегантную терапию во избежание тромбоза стента. В типичном случае - это Аспирин + Клопидогрель (Плавис, Зилт и др.). Спустя 12 месяцев продолжается пожизненный прием Аспирина. При его непереносимости - Клопидогрель.
Помните о крайне важном длительном приеме двойной антиагрегантной терапии после стентирования коронарной артерии. Тромбоз стента - это повторный инфаркт миокарда со всеми вытекающими рисками. В плане убывания силы протективного эффекта от тромбоза стента антиагреганты располагаются следующим образом: Брилинта → Плавикс → дженерики Плавикса (Зилт, Плагрил и др.). Аспирин в качестве монотерапии от тромбоза стента не уберегает!
В отсутствие стентирования больному с перенесенным инфарктом миокарда показан пожизненный прием Аспирина. Антиагрегантная терапия является одним из важнейших патогенетических звеньев лечения ИБС - профилактики тромботических осложнений. Ее игнорирование чревато развитием повторного инфаркта. При этом не имеет значение какой инфаркт миокарда (мелко- или крупноочаговый, с последствиями или без) был перенесен и проводилась ли реваскуляризирующая операция - антиагрегантная терапия показана каждому больному ИБС.
Более сложным кажется выработать мотивацию к приему статина (Аторис, Крестор, Липримар и др.). Дислипидемия встречается не у каждого больных с инфарктом миокарда. Однако если дислипидемия доказана (самый ее распространенный вариант: высокий уровень ЛПНП или (и) низкий уровень ЛПВП) - статинотерапия жизненно необходима. Целевым уровнем ЛПНП являются значения ниже 2,5 ммоль/л; ЛПВН - выше 1,1 ммоль/л. С помощью статинов необходимо добиться такого снижения кровяного холестерина, чтобы по принципу градиента концентрации начался его естественный отток из стенок артерий в кровь (далее в печень, где разрушается). При "нелипидном" атеросклерозе все равно рекомендуется принимать статин (исходя из постулата: "без холестерина - нет атеросклероза").
Следует понимать, что если пациент не борется с такими "липидными" факторами риска, как избыточный вес, неправильное питание (прежде всего, поздний и калорийный ужин), гипергликемия (сахарный диабет), то эффективность статинотерапии будет в разы меньше. Напротив, если указанные факторы риска успешно коррегируются, то уровень кровяного холестерина может нормализоваться сам по себе.
В отсутствие артериальной гипертонии бета-блокаторы постинфарктному больному абсолютно показаны в двух случаях: 1) если в коронарных артериях сохраняются гемодинамически значимые сужения ("пятая ситуация", описанная выше); цель: профилактика стенокардии напряжения и внезапной сердечной смерти;
2) если инфаркт миокарда осложнился хронической сердечной недостаточностью ("четвертая ситуация", описанная выше); цель приема: "оборвать" порочные патофизиологические круги, формирующиеся при сердечной недостаточности. В отсутствие указанных рисков относительным показанием к приему бета-блокаторов является стабильно высокий пульс в покое (выше 70 в минуту). Постинфарктному больному рекомендовано подобрать один из трех бета-блокаторов: бисопролол (торговые названия: Конкор, Нипертен и др.), метапролола сукцинат (торговое название: Беталок, Беталок-Зок) или небиволол (торговые названия: Небилет, Небилонг).
Ингибиторы АПФ изначально были синтезированы и представлены как гипотензивные средства. В этом отношении они себя хорошо зарекомендовали. Позже было установлено, что они эффективны при хронической сердечной недостаточности (в том числе при постинфарктной), поскольку, обрывая порочные патофизиологические круги (как и бета-блокаторы), они замедляют ремоделирование (расширение) левого желудочка. В настоящее время гипотензивный эффект ингибиторов АПФ не столь интересен кардиологам, в связи с присутствием на фармрынке более эффективных и безопасных медикаментов. Однако для лечения сердечной недостаточности ингибиторы АПФ незаменимы ("четвертая и пятая ситуация", описанная выше). Наибольшая доказательная получена на периндоприле (Престариум) и рамиприле (Хартил).
Проблематичной выглядит ситуация с приверженностью к медикаментозному лечению (комплаентностью) среди лиц молодого и среднего возраста, перенесших инфаркт миокарда. Необходимость в пожизненном приеме лекарств, лицами доселе ничем не болевшими, психологически травмирует их. Обозначенный выше "медикаментозный минимум" является кардиологическим постулатом для постинфарктного больного - данные лекарства продлевают жизнь. Однако, если по независящим от больного причинам, он не имеет возможности принимать все указанные препараты, то в порядке убывания клинической значимости (безотносительно к индивидуальным факторам риска) их можно расположить следующим образом: Антиагрегант → Статин → Бета-блокатор → Ингибитор АПФ.
Постинфарктные больные нередко сталкиваются с суровой действительностью - профессиональной дезадаптацией. Речь идет о настороженном отношении работодателя к человеку, перенесшему инфаркт миокарда. И если работа пациента была связана с высокими физическими (рабочие специальности) или эмоциональными нагрузками (руководитель), то существует вероятность, что при прохождении регулярной медицинской комиссии в рамках профосмотра будет вынесен вердикт: негоден. Однако "безусловному комиссованию" подлежат только пациенты из пятой группы. Больным из четвертой группы абсолютно противопоказана профессиональная деятельность, связанная с интенсивными физическими нагрузками. Любой иной вид деятельности (при условии, что инфаркт миокарда не имеет явно инвалидизирующих последствий в виде тяжелой сердечной недостаточности), включая административную работу, пациентам из этой группы не противопоказан. Инфаркт миокарда "без клинико-инструментальных последствий" не является противопоказанием для выполнения прежних профессиональных обязанностей.
Сложно переоценить роль поликлинического кардиолога в реабилитации постинфарктного больного, поскольку прежде всего от него зависит клиническая оценка ситуации (включая легализацию инвалидности) и постулирование "профессионального вердикта". Помимо данных инструментального обследования (прежде всего УЗИ сердца и Холтера) учитывается многое: возраст, переносимость физической нагрузки после инфаркта, психологическая обстановка в семье, эмоциональный настрой на дальнейшую работу самого больного, вероятность успешной борьбы с факторами риска атеросклероза.
Как часто необходимо проходить профилактические обследования сердца после инфаркта миокарда? Все зависит от последствий заболевания. Через 4-6 месяцев после выписки имеет смысл сделать УЗИ сердца и Холтер для оценки систолической функции левого желудочка (есть ли рубцовые поля?) и выявления экстрасистолической аритмии. Данные обследования позволяют ответить на вопрос: каковы ближайшие и отдаленные сердечные риски? Если рисков нет ("инфаркт без последствий"), то рекомендуется наблюдение у кардиолога с частотой раз в год и ежегодная сдача анализа крови на холестерин. В подобной ситуации необходимость в регулярных инструментальных обследованиях отсутствует.
В случае перенесенного крупноочагового инфаркта миокарда, объективные последствия которого сохраняются пожизненно ("инфаркт видимый при УЗИ"), помимо регулярного посещения кардиолога, необходимо минимум раз в год делать УЗИ сердца, ЭКГ, Холтер и сдавать кровь на холестерин. Выполнение этих диагностик позволит оценить эффективность лечения в динамике и провести стратификацию сердечно-сосудистого риска. При наличии высокого риска необходимо рассмотреть возможность использования различных современных инвазивных лечебных методик по показаниям: плановая реваскуляризация, аневризмэктомия, имплантация кардиовертера-дефибриллятора, ресинхронизирующая терапия и др. Что касается целесообразности проведения плановой коронарографии, то следует помнить, что как и любая инвазивная манипуляция, она не лишена риска осложнений, в том числе жизнеугрожающих. Поэтому прибегать к ней стоит только при клиническом ухудшении самочувствия. В случае благоприятного течения заболевания коронарографию имеет смысл выполнять не чаще, чем 1 раз в 3-5 лет.
Нерешенным остается вопрос, о необходимости планового стентирования коронарной артерии с пограничным стенозом в 60-70%. Следует помнить, что установка стента сопровождается риском его последующего тромбоза (несмотря на прием антиагрегантов) с непредсказуемыми последствиями. Поэтому стентирование бессимптомных "пограничных" по гемодинамической значимости стенозов скорее не показано. При коррекции образа жизни данные стенозы могут больше не прогрессировать.
Высокий риск инфаркта миокарда в пожилом возрасте связан не столько с самим процессом старения, сколько с особенностями подсознательного восприятия старости. Основной причиной стремительного прогрессирования системного атеросклероза у пожилых людей (конечно, при условии отсутствия других факторов риска) является хронически пониженный эмоциональный(гипотимия). Причины разные, но объединяет их то, что все они обусловлены старческим бытием:
- инволюционная меланхолия;
- восприятие выхода на пенсию как личностной драмы, в связи с потерей высокого социального статуса ("шок отставки") или привычного уклада жизни;
- иррациональные установки пожилого человека: "впереди ничего нет", "жизнь закончилась" и т.п.;
- потеря внутрисемейного ранга как причина эмоционального переживания ("отношение к старику, как к объекту, а не субъекту");
- проживание в одиночестве;
- возрастные физические недуги ("все болит"), ухудшающие эмоциональное самочувствие;
- отсутствие смысла жизни.
Это является ответом на вопрос, который часто задают сами больные или их родственники: "откуда взялся инфаркт, если никогда ничем не болел"?
Лечение и реабилитация пожилого постинфарктного субъекта имеет свои особенности. С одной стороны, врачу можно надеется на высокую комплаентность (приверженность к медикаментозному лечению) в связи с педантичным отношением стариков к своему здоровью и невысоким темпом жизни. С другой стороны, в пожилом возрасте часто имеет место целый "букет" хронических заболеваний, которые могут затруднять прием необходимых медикаментов из-а феномена полипрагмазии. Например, прием ингибиторов АПФ на фоне хронической почечной недостаточности может усугубить течение последней. Или, часто встречающиеся в старости, сердечные блокады могут быть препятствием для приема бета-блокаторов. Аспирин и статин являются обязательной составной частью медикаментозного лечения у пожилого постинфарктного пациента. Статины в этом смысле - единственное лекарство "от старения сосудов". Отсутствие дислипидемии не должно служить поводом для отказа от их приема.
Еще одной особенностью инфаркта миокарда в старости является то, что очень часто он развивается на фоне многососудистого, кальцинированного поражения коронарных артерий. Это приводит к невозможности выполнения операции стентирования или к необходимости многократного стентирования. В подобной ситуации показана шунтирующая операция, однако из-за высокого операционного риска в ней нередко отказывают. "Суженные" или окклюзированные артерии предопределяют сохранение высоких постинфарктных сердечных рисков: нестабильной стенокардии, повторного инфаркта, внезапной смерти.
Выделяют несколько социально-психологических типов старения, наполняющих жизнь смыслом и обладающих протекцией в отношении атеросклероза (расположены в порядке убывания силы антиатерогенного эффекта):
1-й тип - активная творческая старость, когда пожилые люди продолжают участвовать в общественной жизни, сохраняя социальные и профессиональные связи.
2-й тип - пенсионеры занимаются теми делами, на которые раньше у них не было времени: самообразование, путешествия, отдых, развлечения.
3-й тип - жизненная энергия направлена на семейные заботы: помощь детям в воспитании внуков, забота о больном родственнике и т.п.
4-й тип - смысл жизни заключается в заботе о собственном здоровье, с чем связаны разнообразные формы активности и моральные установки.
Аэмоциональная, бездеятельная, эгоистичная старость всегда сопровождается стремительным прогрессированием атеросклероза. Его финал: сосудистая катастрофа.
Заключение: общие рекомендации больному, перенесшему инфаркт миокарда.
- Переосмыслить свою жизнь. Кто вы? Зачем пришли в этот мир? Куда идете?
- С помощью врача выяснить, каков патогенез вашего атеросклероза: преимущественно липидный или преимущественно нелипидный?
- Сотрудничать с лечащим кардиологом. При гармоничном отношении к болезни и к последующему лечению визиты к врачу будут редкими и необременительными.
- Обязательно принимать необходимые медикаменты (к сожалению для пациента - пожизненно). "Нервические натуры", для которых прием обилия лекарств неприемлем, могут ограничиться сочетанием антиагреганта и статина.
- Вести активный образ жизни, в тех рамках, которые допускает текущая "постинфарктная конъюнктура".
- Пожилым пациентам следует задуматься о психодинамике старческого атеросклероза: необходимо, вопреки возрасту, придать жизни смысл. Родственники могут им в этом помочь.